
下列有关实验叙述不正确的是( )

A.图A中顾虑适用于分离固-液混合物
B.图B中利用渗析可将胶体粒子与杂志的小分子、离子分离开
C.图C中萃取可用来将固体或液体中的某溶质用萃取剂提取出来
D.图D中只有液态胶体才能产生丁达尔效应
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都属于离子型碳化物。请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
A.ZnC2水解生成乙烷 B.Al4C3水解生成丙炔
C.Mg2C3水解生成丙炔 D.Li2C2水解生成乙烯
查看答案和解析>>
科目:高中化学 来源:2015届安徽省铜陵市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是: ( )
A.若配制100mL 0.5mol/L Na2SO4溶液,则需要称量Na2SO4·10H2O的质量为7.1g
B.80g NaOH溶于1L水中,则溶质的物质的量浓度为2mol/L
C.1mol氢气和1mol氦气中,所含的分子数相同、原子数相同、质量也相同
D.1mol Al与足量的稀盐酸反应变成Al3+,失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三第一次联考化学试卷(解析版) 题型:填空题
(8分)A、B、C、D四种元素均为元素周期表中的短周期元素,原子序数依次增大,A元素基态原子中p电子数是s电子数的二分之一,B元素最高价氧化物的水化物与其氢化物能够反应生成一种盐,C元素与D元素能形成原子个数比为1:2和1:1的两种常见离子化合物。
(1)A、B、C三种元素的电负性从大到小的顺序是_______________(填元素符号)
(2)D元素原子核外的电子排布式是______________.
(3)B元素与D元素形成的化合物DB2的晶体类型为____________.B2中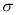 键与
键与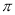 键数目之比为_________________.
键数目之比为_________________.
(4)A、C、D三种元素形成的原子个数比为A:C:D=1:2:1简单化合物的水溶液呈碱性,其原因为(用离子方程式表示):___________________________________________.
(5)已知:B2(g)+2C2(g)=2BC2(g) △H=+67.6kJ·mol-1
B2H4(g)+C2(g)=B2(g)+2H2C(g) △H=-534kJ·mol-1
请写出BC2(g)与B2H4(g)反应生成B2(g)和H2C(g) 的热化学方程式:___________________.
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三第一次联考化学试卷(解析版) 题型:选择题
已知反应:A(g)+3B(g)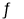 2C(g),
2C(g),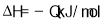 。在容积为1L的固定体积的容器中充入1molA、3molB,各物质浓度随时间变化的曲线如图所示,下列说法错误的是( )
。在容积为1L的固定体积的容器中充入1molA、3molB,各物质浓度随时间变化的曲线如图所示,下列说法错误的是( )
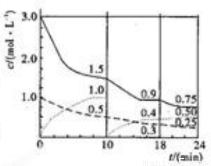
A.第18-24分钟用B物质表示的反应速率为0.025mol·L-1·min-1
B.容器中气体的平均摩尔质量不再发生变化时反应达到了平衡状态
C.前10分钟内反应放出的热量为Q/2kJ
D.第18分钟时改变的条件是增大了压强
查看答案和解析>>
科目:高中化学 来源:2015届安徽省皖南八校高三第一次联考化学试卷(解析版) 题型:实验题
(15分)纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油扭、涂料、密封胶与胶粘剂等行业。在浓CaCl2,溶液中通人NH3和CO2,可以制得纳米级碳酸钙。某校学生实验小组设计下图所示装置,制取该产品。D中装有他稀硫酸的脱脂棉.图中夹持装置已略去。
I.可选用的药品有:a.石灰石b.饱和氯化钙溶液c.6 mol/L盐酸d.氯化铵固体e.氢氧化钙固体。
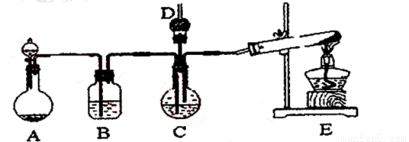
(1)A中制备气体时,所需药品是(选填字母序号)______________;
(2)B中盛有_________溶液,其作用是_____________;
(3)写出制取氨气的化学方程式_____________________;
(4)在实验过程中,向C中通入气体是有先后顺序的,应先通入的气体是_____(写化学式)
(5)检验D出口处是否有氨气逸出的方法是_______________________;
(6)写出制取纳米级碳酸钙的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源:2015届安徽省皖南八校高三第一次联考化学试卷(解析版) 题型:选择题
下列大小顺序排列不正确的组合是
A.气态氢化物的稳定性:HCl>HBr>HI
B.离子半径:S2->Na+>O2-
C.酸性:HClO4>H2SO4>H3PO4
D.熔点:SiO2>NaCl>干冰
查看答案和解析>>
科目:高中化学 来源:2015届安徽省江淮十校高三11月联考化学试卷(解析版) 题型:选择题
电导率可用于衡量电解质溶液导电能力的大小。室温下,用0.100 mol·L-1 NH3·H2O滴定10 mL浓度均为0.100 mol·L-1HCl和CH3COOH的混合液,电导率曲线如图所示。
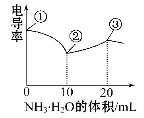
下列说法正确的是
A.①溶液中c(H+)为0.200 mol·L-1
B.溶液温度高低为①>③>②
C.③点溶液中有c(Cl—)>c(CH3COO—)
D.③点后因离子数目减少使电导率略降低
查看答案和解析>>
科目:高中化学 来源:2015届宁夏银川市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.SiO2具有较好的导电性,可用于制造半导体材料
B.H2O2是一种绿色氧化剂,可氧化酸性高锰酸钾而产生O2
C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
D.Mg在空气中燃烧发出耀眼的白光,可用于制作信号弹
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com