
����Ŀ���ҹ�ÿ������ķϾ�Ǧ����Լ330��֡��Ӻ�Ǧ���ϣ�PbSO4��PbO2��PbO�ȣ��л���Ǧ��ʵ��Ǧ�������������ش�һ�ֻ���Ǧ�Ĺ����������£�

(1)Ǧ���طŵ�ʱ��PbO2��____����
(2)����I����֪��PbSO4��PbCO3���ܽ��(20��)��ͼl��Na2SO4��Na2CO3���ܽ�ȼ�ͼ2��

�ٸ���ͼlд������I�����ӷ���ʽ��__________��
�����������е��¶�Ӧ������40�棬���¶Ƚ��ͣ�PbSO4��ת�������½�������ͼ2�����Ϳ���ԭ��
i���¶Ƚ��ͣ���Ӧ���ʽ��ͣ� ii��____���������һ�ֺ������ͣ���
���������������¶ȵ���40�棬���ù����У����н϶�Na2SO4���ʣ�ԭ����____��
(3)���̢�����Ӧ2PbO2+H2C2O4=2PbO+H2O2+2CO2����ʵ���м��д���O2�ų����Ʋ�PbO2������H2O2��ͨ��ʵ��֤ʵ����һ�Ʋ⡣ʵ�鷽����____��
����֪��PbO2Ϊ�غ�ɫ���壻PbOΪ�Ȼ�ɫ���壩
(4)���̢�PbO��Ʒ�ܽ���HCl��NaCl�Ļ����Һ�У��õ���Na2PbCl4�ĵ��Һ�����Na2PbCl4��Һ������Pb����ͼ3��
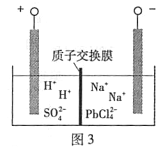
�������ĵ缫��Ӧʽ��____________��
�ڵ��һ��ʱ���PbCl2'Ũ�ȼ����½���Ϊ�˻ָ���Ũ����ʵ�����ʵ�ѭ�����ã���������ȡ�ķ�����_______��
���𰸡� �� PbSO4 (s) +CO32- (aq)![]() PbCO3 (s) +SO42- (aq) Na2SO4��Na2CO3Ũ�Ƚ��ͣ���Ӧ���ʽ��� �¶ȵ���40��ʱ���¶Ƚ��ͣ�ƽ�⡰Na2SO4(s)
PbCO3 (s) +SO42- (aq) Na2SO4��Na2CO3Ũ�Ƚ��ͣ���Ӧ���ʽ��� �¶ȵ���40��ʱ���¶Ƚ��ͣ�ƽ�⡰Na2SO4(s)![]() 2Na+(aq) +SO42- (aq)�������ƶ��������϶�Na2SO4�������� ȡ����PbO2���Թ��У������еμ�H2O2��Һ��������ʹ������ľ����ȼ�����壬ͬʱ�غ�ɫ�����Ϊ�Ȼ�ɫ��֤ʵ�Ʋ���ȷ PbCl42-+2e-=Pb+4Cl- ��������������PbO��Ʒ
2Na+(aq) +SO42- (aq)�������ƶ��������϶�Na2SO4�������� ȡ����PbO2���Թ��У������еμ�H2O2��Һ��������ʹ������ľ����ȼ�����壬ͬʱ�غ�ɫ�����Ϊ�Ȼ�ɫ��֤ʵ�Ʋ���ȷ PbCl42-+2e-=Pb+4Cl- ��������������PbO��Ʒ
��������(1)Ǧ���طŵ�ʱ��PbO2�õ����ӣ���������(2)�ٸ���ͼl��֪̼��Ǧ�����ܣ�����ݳ���ת����֪����I�����ӷ���ʽΪ PbSO4(s)+CO32- (aq)![]() PbCO3(s)+SO42-(aq)���ڸ���ͼ2��֪�¶Ƚ���ʱNa2SO4��Na2CO3Ũ�Ƚ��ͣ���Ӧ���ʽ��ͣ���˵���ת�����½������¶ȵ���40��ʱ���¶Ƚ��ͣ�ƽ�⡰Na2SO4(s)
PbCO3(s)+SO42-(aq)���ڸ���ͼ2��֪�¶Ƚ���ʱNa2SO4��Na2CO3Ũ�Ƚ��ͣ���Ӧ���ʽ��ͣ���˵���ת�����½������¶ȵ���40��ʱ���¶Ƚ��ͣ�ƽ�⡰Na2SO4(s)![]() 2Na+(aq)+SO42-(aq)�������ƶ��������϶�Na2SO4�������ʡ�(3)���PbO2������H2O2�����Ȼ����PbO��������ɫ���жϣ���ȡ����PbO2���Թ��У������еμ�H2O2��Һ��������ʹ������ľ����ȼ�����壬ͬʱ�غ�ɫ�����Ϊ�Ȼ�ɫ��֤ʵ�Ʋ���ȷ��(4)�����������õ����ӵĻ�ԭ��Ӧ����缫��Ӧʽ��PbCl42-+2e-=Pb+4C1-��������PbO���ܽ���HCl��NaCl�Ļ����Һ�У��õ���Na2PbCl4�ĵ��Һ�����Ϊ�˻ָ���Ũ����ʵ�����ʵ�ѭ�����ã���������ȡ�ķ����Ǽ�������������PbO��Ʒ��
2Na+(aq)+SO42-(aq)�������ƶ��������϶�Na2SO4�������ʡ�(3)���PbO2������H2O2�����Ȼ����PbO��������ɫ���жϣ���ȡ����PbO2���Թ��У������еμ�H2O2��Һ��������ʹ������ľ����ȼ�����壬ͬʱ�غ�ɫ�����Ϊ�Ȼ�ɫ��֤ʵ�Ʋ���ȷ��(4)�����������õ����ӵĻ�ԭ��Ӧ����缫��Ӧʽ��PbCl42-+2e-=Pb+4C1-��������PbO���ܽ���HCl��NaCl�Ļ����Һ�У��õ���Na2PbCl4�ĵ��Һ�����Ϊ�˻ָ���Ũ����ʵ�����ʵ�ѭ�����ã���������ȡ�ķ����Ǽ�������������PbO��Ʒ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������������������Ĵ�������������������о����ȵ����⡣
��������β���е�NO��CO�������ڼ���PM2.5���ŷš���֪������Ϣ��
2CO(g)��2NO(g)![]() 2CO2(g)��N2(g)����H1����748kJ��mol��1
2CO2(g)��N2(g)����H1����748kJ��mol��1
2CO(g)��O2(g)===2CO2(g)����H2����565kJ��mol��1
(1)��һ��������N2��O2��ת��ΪNO��д���÷�Ӧ���Ȼ�ѧ����ʽ��_________��
(2)Ϊ�о���ͬ�����Է�Ӧ��Ӱ�죬�ں��������£���2L�����ܱ������м���0.2molNO��0.4mol CO���ڴ������ڵ������·�����Ӧ��10minʱ��Ӧ�ﵽƽ�⣬���10min��v(NO)��7.5��10��3mol��L��1��min��1����ƽ���n(CO)��________mol�����ڸ�ƽ�������˵����ȷ����________��
a������ѹǿ��ƽ��һ�������ƶ�
b�������������䣬�����¶ȣ���ѧ��Ӧ����һ������
c�������������䣬����Ϊ�ں�ѹ�����н��У�CO��ƽ��ת���ʱȺ��������´�
d���ﵽƽ���v��(NO)��2v��(N2)
(3)����������ͬ��t minʱ��ͬ�¶��²��NO��ת������ͼ��ʾ��

A��ķ�Ӧ�ٶ�v��________(�����������������)v����A��B���㷴Ӧ��ƽ�ⳣ���ϴ����________(�A����B��)��
(4)��֪HNO2�ĵ��볣��Ka��7.1��10��4mol��L��1��
NH3��H2O�ĵ��볣��Kb��1.7��10��5mol��L��1
��0.1mol��L��1NH4NO2��Һ������Ũ���ɴ�С��˳����____________________________��
������NO2-ˮ�ⷴӦ��ƽ�ⳣ��Kh��________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƴ��˵���ҩ�����У���������ǻ�Ϭţ�ǵ��������٣�����ȱ����ζҩ����Ч������½�������Ч����֪����Ľ���Ҫ��������ϸ���Ľǻ������ԣ���������ɵģ�������ǵȵ���Ч�ɷ��������
A. ������Ե����� B. DNA
C. ��Ԫ���� D. ����Ԫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���Ũ�ȵ�NaOH��Na2CO3�Ļ����Һ�м���ϡ���ᡣ�������ӷ���ʽ����ʵ���������(����)
A. OH����CO![]() ��2H��===HCO
��2H��===HCO![]() ��H2O
��H2O
B. 2OH����CO![]() ��3H��===HCO
��3H��===HCO![]() ��2H2O
��2H2O
C. 2OH����CO![]() ��4H��===CO2����3H2O
��4H��===CO2����3H2O
D. OH����CO![]() ��3H��===CO2����2H2O
��3H��===CO2����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ա����������CO2�����з�Ӧ��������ʵ�ֿռ�վ��O2��ѭ�����á�
sabatior��Ӧ��CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
ˮ��ⷴӦ��2H2O(l)![]() 2H2(g) + O2(g)
2H2(g) + O2(g)
(1)��ԭ������nCO2��nH2=1:4�����ܱ������з���Sabatier��Ӧ�����H2O(g)�����ʵ����������¶ȵĹ�ϵ��ͼ��ʾ(���߱�ʾƽ������)��
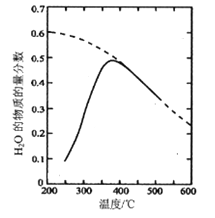
�ټ�֪H2(g)��CH4(g)��ȼ���ȷֱ�ΪA kJ/mol��BkJ/mol�� H2O(l)=H2O(g) ��H =C kJ��mol������Sabatier��Ӧ�ġ�H=___kJ/mol��
���¶ȹ�����;������ڸ÷�Ӧ�Ľ��У�ԭ����________��
��200��ﵽƽ��ʱ��ϵ����ѹǿΪp���÷�Ӧƽ�ⳣ��Kp�ļ���ʽΪ________��(���ػ�����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)
(2)Sabatier��Ӧ�ڿռ�վ����ʱ�����д�ʩ�����CO2ת��Ч�ʵ���______(����)��
A.�ʵ���ѹ B.��������ıȱ����
C.��Ӧ��ǰ�μ��ȣ������ȴ D.���ԭ������CO2��ռ����
E.�������Ʒ�Ӧ�������������
(3) һ���µ�ѭ�����÷�������Bosch��ӦCO2(g)+2H2(g)![]() C(s)+2H2O(g)����Sabatier��Ӧ��
C(s)+2H2O(g)����Sabatier��Ӧ��
��250�棬�����Ϊ2L�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��0.08molH2��0.04molCO2����Bosch ��ӦCO2(g)+2H2(g)![]() C(s)+2H2O(g) �� H
C(s)+2H2O(g) �� H
������Ӧ��ʼ��ƽ��ʱ�¶���ͬ(��Ϊ250��)����÷�Ӧ������ѹǿ(P)��ʱ��(t)�ı仯��ͼI ����a��ʾ�����H___ 0(�>����<����ȷ����) ��������������ͬ�����ı�ijһ����ʱ�������ѹǿ(P)��ʱ��(t)�ı仯��ͼI ����b��ʾ����ı��������______________��
��ͼII�Ǽס�����ͬѧ���������Ӧƽ�ⳣ���Ķ���ֵ(lgK)���¶ȵı仯��ϵ��������ȷ��������____________(��ס����ҡ�)��mֵΪ____________��

��Bosch��Ӧ�����ڸ����²���������ԭ����__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʢ����ˮ����֧�Թ��зֱ����ƾ������Ȼ�̼�ͱ������ã���������������ȷ�Ľ����ǣ�������

A. �ټ���CCl4 �ڼ��˱� �ۼ��˾ƾ�
B. �ټ��˱� �ڼ���CCl4 �ۼ��˾ƾ�
C. �ټ��˾ƾ� �ڼ���CCl4 �ۼ��˱�
D. �ټ��˱� �ڼ��˾ƾ� �ۼ���CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ����ȡ������Ϊ50 mL��A��B����NaOH��Һ�У��ֱ�ͨ��һ������CO2����ϡ�͵�100 mL��
(1)��NaOH��Һ��ͨ��һ������CO2����Һ�����ʵ���ɿ����Ǣ�________����________����________����________��

(2)��ϡ�ͺ����Һ����μ���0.1 mol ��L��1�����ᣬ����CO2�����(��״��)����������������ϵ��ͼ��ʾ��
��A���߱�����ԭ��Һͨ��CO2���������������ᷴӦ����CO2����������________mL(��״��)��
��B���߱�����ԭ��Һͨ��CO2��������Һ�����ʵĻ�ѧʽΪ______________________��
��ԭNaOH��Һ�����ʵ���Ũ��Ϊ_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������׳��̷�(FeSO4 7H2O)���ظ����ƾ����׳ƺ췯��(Na2Cr2O7��2H2O)�����Ƕ�����Ҫ�Ļ�����Ʒ����ҵ���Ը�����[��Ҫ�ɷ���[Fe(CrO2)2]Ϊԭ���Ʊ��̷��ͺ췯�ƵĹ���������ͼ��ʾ��
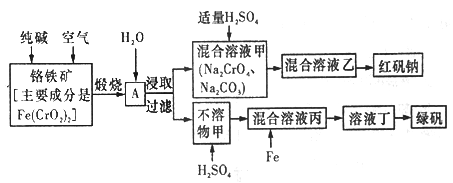
��ش��������⣺
(1)��֪Fe(CrO2)2�и�Ԫ�صĻ��ϼ�Ϊ+3�ۣ���Fe(CrO2)����Ԫ�صĻ��ϼ�Ϊ______________��
(2)��ѧ�Ͽɽ�ijЩ��д�����������ʽ����Na2SiO3д��Na2O��SiO2����Fe(CrO2)2��д��__________��
(3)���ո�����ʱ����ʯ�е�Fe(CrO2)2ת��ɿ�����ˮ��Na2CrO4����Ӧ�Ļ�ѧ����ʽ���£�
4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4+8CO2
2Fe2O3+8Na2CrO4+8CO2
�ٸ÷�Ӧ�л�ԭ���������������ʵ���֮��Ϊ________________��
��Ϊ�˼ӿ�÷�Ӧ�ķ�Ӧ���ʣ��ɲ�ȡ�Ĵ�ʩ��_________________(��һ�ּ���)��
�ȼ�֪CrO42-��������Ũ�Ȳ�ͬ��������Һ���в�ͬ�ķ�Ӧ���磺
2CrO42-+2H+=Cr2O72-+H2O 3CrO42-+4H+=Cr3O102-+2H2O
���������Һ���м����������������ԭ����________________��
�ڻ����Һ�������ʵĻ�ѧʽΪ______________________��
(5)д��Fe������Һ����Ӧ����Ҫ���ӷ���ʽ_________________��������Һ������Fe3+�ķ����ǣ�_____________������Һ�����̹���ʵ�����Ϊ����Ũ����___________�����ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�����N2O5��CCl4�з�����Ӧ��2N2O5===4NO2��O2��N2O5��Ũ���淴Ӧʱ��(t)�ı仯���±�����0��10 s����ƽ����Ӧ����Ϊ(����)
t/s | 0 | 5 | 10 | 15 |
N2O5/(mol��L��1) | 0.82 | 0.40 | 0.32 | 0.28 |
A. v(N2O5)��0.032 mol��L��1
B. v(N2O5)��0.050 mol��L��1
C. v(N2O5)��0.050 mol��L��1��s��1
D. v(N2O5)��0.032 mol��L��1��s��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com