
| A. | CO2和NaOH完全反应生成碳酸氢钠 | |
| B. | 反应所得溶液呈酸性 | |
| C. | HCO3-的电离程度大于HCO3-的水解程度 | |
| D. | 存在的平衡体系只有:HCO3-+H2O?H2CO3+OH-,HCO3-?H++CO32- |
分析 n(CO2)=$\frac{11.2L}{22.4L/mol}$=0.05mol,n(NaOH)=$\frac{2g}{40g/mol}$=0.05mol,二者的物质的量之比为1:1,恰好发生反应:NaOH+CO2=NaHCO3,得到NaHCO3溶液,NaHCO3溶液中HCO3-离子水解程度大于其电离程度,导致溶液呈碱性.
解答 解:A.n(CO2)=$\frac{11.2L}{22.4L/mol}$=0.05mol,n(NaOH)=$\frac{2g}{40g/mol}$=0.05mol,二者的物质的量之比为1:1,恰好发生反应:NaOH+CO2=NaHCO3,得到NaHCO3,故A正确;
B.NaHCO3溶液中HCO3-离子水解程度大于其电离程度,导致溶液呈碱性,故B错误;
C.HCO3-的电离程度小于HCO3-的水解程度,故C错误;
D.溶液中还存在水的电离平衡:H2O?OH-+H+,故D错误,
故选:A.
点评 本题考查化学方程式计算、盐类水解等,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-(Ea-Eb) kJ/mol | |
| B. | 某温度下,氯化钠在水中的溶解度是20 g,则该温度下的饱和氯化钠溶液溶质的质量分数为20% | |
| C. | 将0.2 mol/L 的CH3COOH 溶液与0.1 mol/L 的NaOH 溶液等体积混合后,溶液中有关粒子的浓度满足下列关系:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| D. | 将浓度为0.1 mol/L HF 溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3可用作耐火材料,硅酸钠是制备木材防火剂的原料 | |
| B. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜合金 | |
| C. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 | |
| D. | 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+Cl2→CH2ClCH2Cl | B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | ||
| C. | 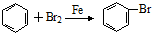 | D. | 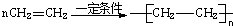 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定HCl和NaOH反应中和热,应测量盐酸、NaOH起始温度和反应后终止温度 | |
| B. | 1mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热△H=+285.8 kJ/mol | |
| C. | 1 mol C与O2反应生成1mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ/mol | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Ag+、Cl-、NO3- | B. | K+、SO42-、Na+、Cl- | ||
| C. | Ba2+、Na+、OH-、CO32- | D. | Al3+、NH4+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | Fe2+ | C. | Cu2+和Fe2+ | D. | Fe3+和Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的密度是否变化 | |
| B. | 容器内的压强是否变化 | |
| C. | 容器中A的浓度是否变化 | |
| D. | 容器中C、D的物质的量之比是否变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com