
【题目】利用如图实验装置进行相关实验,能得出相应实验结论的是( )
a | b | c | 实验结论 |
| |
A | 浓醋酸 | CaCO3 | C6H5ONa溶液 | 酸性:碳酸>苯酚 | |
B | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯和液溴发生取代反应 | |
C | 浓盐酸 | 酸性KMnO4溶液 | 碘化钾溶液 | 氧化性:Cl2>I2 | |
D | 饱和食盐水 | 电石 | 酸性KMnO4溶液 | 乙炔具有还原性 |
A.AB.BC.CD.D
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】利用下列实验装置能完成相应实验的是
选项 | 装置图 | 实验目的 |
A |
| 收集干燥的HCl |
B |
| 除去CO2中含有的少量HCl |
C |
| 收集H2、NH3、CO2、Cl2、HCl、NO、NO2等气体 |
D |
| 检查装置的气密性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.糖类、油脂和蛋白质都是天然高分子化合物
B.苯、苯乙炔、甲苯、苯酚分子中所有原子都共平面
C.分子式为C5H12O且能与钠反应产生氢气的有机物的同分异构体有8种
D.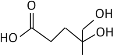 是乙酸的同系物,能和碳酸钠反应
是乙酸的同系物,能和碳酸钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“结晶玫瑰”具有强烈的玫瑰香气,属于结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。“结晶玫瑰”的化学名称为乙酸三氯甲基苯甲酯,通常用三氯甲基苯基甲醇和醋酸酐为原料制备。
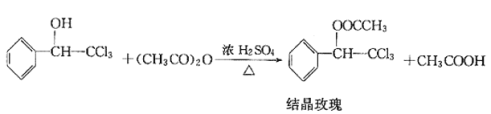
已知:
物质 | 在乙醇中的溶解性 | 在水中的溶解性 | 熔点℃ |
三氯甲基苯基甲醇 | 溶 | 不溶 | — |
醋酸酐 | 溶 | 溶 | -73 |
结晶玫瑰 | 溶 | 不溶 | 88 |
醋酸 | 易溶 | 易溶 | 16.6 |
部分实验装置以及操作步骤如下:
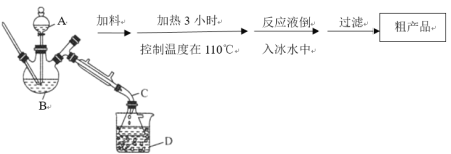
请根据以上信息,回答下列问题:
(1)装置中仪器B的名称是___________。
(2)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌。待混合均匀后,最适宜的加热方式为油浴加热,用油浴加热的理由是_______________。有同学认为装置中A仪器也可改为另一种漏斗,该漏斗的名称是___________,它的作用是____________。
现有同学设计如下方案把粗产品进行提纯。
(3)①将粗产品溶解在________(填“水”、“乙醇”或“粗产品滤液”)中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解,得到无色溶液。然后将所得溶液经过__________(填操作方法)析出白色晶体,整个过程中不需要用到的仪器是_______(选择相应字母填空)。
A.冷凝管 B.烧杯 C.蒸发皿 D.玻璃棒
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,请列举一种常见的实验室干燥的方法_______。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,实验现象为__________。
(4)ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰bg,则产率是_________。(用含a、b的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 先将
先将![]() 溶于水制成
溶于水制成![]() 溶液,然后取出
溶液,然后取出![]() 溶液滴加
溶液滴加![]() 溶液,整个过程中利用
溶液,整个过程中利用![]() 数据采集器测得溶液的
数据采集器测得溶液的![]() 变化曲线如图所示(实验过程中不考虑
变化曲线如图所示(实验过程中不考虑![]() 的挥发和
的挥发和![]() 的分解)。下列说法正确的是
的分解)。下列说法正确的是
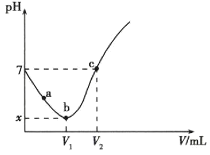
A.![]() 过程中,是氯气溶于水的过程,
过程中,是氯气溶于水的过程,![]() 和水的电离程度均不断增大
和水的电离程度均不断增大
B.![]() 点溶液中
点溶液中![]() 接近于
接近于![]()
C.![]() ,溶液中
,溶液中![]()
D.滴加![]() 溶液的体积为
溶液的体积为![]() 时,
时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关能量转化的说法不正确的是
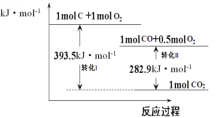
A.25℃时,碳的标准燃烧热:△H=-393.5kJ·mol-1
B.转化II的热化学方程式为:2CO(g)+O2(g)=2CO2(g)△H=-565.8kJ·mol-1
C.在反应C(s)+O2(g)=CO2(g)中,反应物的总键能大于生成物的总键能
D.由碳转化为一氧化碳的热化学方程式为:2C(s)+O2(g)=2CO(g)△H=-221.2kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某研究性学习小组用粗铜(含杂质Fe)与过量氯气反应得到固体,用稀盐酸溶解,然后加试剂调节溶液的pH,经系列操作可得氯化铜晶体。请回答:
(1)电解精炼粗铜时,阴极发生的电极反应为__________。
(2)调节溶液pH的合适试剂为__________。
A.CuO B.Na2CO3 C.Cu2(OH)2CO3 D.稀氨水
(3)在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热后生成CuCl沉淀,写出离子方程式__________。
Ⅱ.某无机化合物A的相对分子质量为184。在一定条件下,SCl2与氨完全反应生成A和淡黄色单质B及离子化合物X,且X的水溶液的pH<7。将18.4gA隔绝空气加强热可得到12.8gB和气体单质C,单质C在标准状况下的密度为1.25g·L-1。请回答下列问题:
(4)A中所含的元素为__________(用元素符号表示)。
(5)写出A隔绝空气加强热的反应方程式__________。
(6)写出SCl2与氨反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com