
【题目】下列说法正确的是
A. 等物质的量浓度的NH4HSO4溶液和NaOH溶液等体积混合,溶液中各离子浓度大小关系为c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B. 常温下电离常数为Ka的酸HA的溶液中c(H+)=![]() mol/L
mol/L
C. 常温下同浓度的强酸和强碱溶液等体积混合后,由水电离出的c(H+)=10-7mol/L
D. 已知298K时氢氰酸(HCN)的Ka=4.9×10-10,碳酸的Ka1=4.4×10-7、Ka2=4.7×10-11,据此可推测出将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
【答案】A
【解析】A. 等物质的量浓度的NH4HSO4溶液和NaOH溶液等体积混合,发生的反应为H++OH-![]() H2O,而且中和反应恰好完全进行,形成等浓度的Na2SO4和(NH4)2SO4的混合溶液,NH4+水解使溶液呈酸性,形成溶液中各离子浓度大小关系为c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故A正确;B. 常温下电离常数为Ka的酸HA的溶液中Ka=
H2O,而且中和反应恰好完全进行,形成等浓度的Na2SO4和(NH4)2SO4的混合溶液,NH4+水解使溶液呈酸性,形成溶液中各离子浓度大小关系为c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故A正确;B. 常温下电离常数为Ka的酸HA的溶液中Ka= ,c(H+)=
,c(H+)=![]() mol/L,故B错误;C. 酸与碱的元酸可以不同,所以常温下同浓度的强酸和强碱溶液等体积混合后,溶液可以呈酸性或碱性,此时由水电离出的c(H+)<10-7mol/L,故C错误;D. 碳酸的Ka2=4.7×10-11<HCN的Ka=4.9×10-10<碳酸的Ka1=4.4×10-7,将氢氰酸加入到碳酸钠溶液中,HCN+ Na2CO3=NaCN+NaHCO3,不能观察到有气泡产生,故D错误。故选A。
mol/L,故B错误;C. 酸与碱的元酸可以不同,所以常温下同浓度的强酸和强碱溶液等体积混合后,溶液可以呈酸性或碱性,此时由水电离出的c(H+)<10-7mol/L,故C错误;D. 碳酸的Ka2=4.7×10-11<HCN的Ka=4.9×10-10<碳酸的Ka1=4.4×10-7,将氢氰酸加入到碳酸钠溶液中,HCN+ Na2CO3=NaCN+NaHCO3,不能观察到有气泡产生,故D错误。故选A。


科目:高中化学 来源: 题型:
【题目】(16分)雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中的主要离子方程式为 。
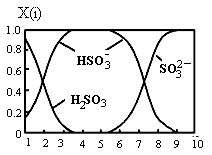 (2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
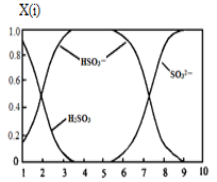
①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下反应的离子方程 式 , 。
(4)装置Ⅲ还可以使Ce4+再生,其原理如图所示。①生成Ce4+从电解槽的 (填字母序号)口流出。②写出阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液是一种常见的强酸,s通常是难溶于水的混合物.上述物质的转化关系如图所示.下列说法正确的是( ) 
A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据外媒报道,WirthResearch公司公布了其用轻型氢燃料电池作为主要能源的无人空中系统(UAS)的设计,该轻型氢燃料电池比普通理离子电池具有更高的能量密度(能量密度是指单位体积或重量可以存储的能量多少)。用吸附了H2的碳纳米管等材料制作的二次电池的原理如下图所示。该电池的总反应为H2+2NiO(OH) ![]() 2Ni(OH)2,已知:6NiO(OH)+NH3+H2O+OH-=6Ni(OH)2+NO2-。下列说法不正确的是
2Ni(OH)2,已知:6NiO(OH)+NH3+H2O+OH-=6Ni(OH)2+NO2-。下列说法不正确的是
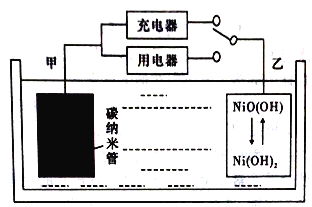
A. 碳纳米管吸附H2的密度越大,电池的能量密度越高
B. 电池可以用KOH溶液、氨水等作为电解质溶液
C. 放电时.乙电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
D. 充电时,电池的碳电极与直流电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列叙述不正确的是( ) 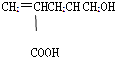
A.1mol该有机物能与足量金属钠反应放出1molH2
B.能与乙醇发生酯化反应
C.1mol该有机物在催化剂作用下最多能与1molH2发生还原反应
D.1mol该有机物能与足量NaHCO3溶液反应放出2 molCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 失电子多的金属还原性强
B. 金属阳离子被还原不一定得到金属单质
C. 某元素从化合态到游离态,该元素一定被还原
D. 金属单质在反应中只能作还原剂,非金属单质只能作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置(夹持装置已省略)制取和收集纯净、干燥的氨气,并探究氨气的性质。

(1)如何检验装置I的气密性?___________________。
(2)利用装置I制取氨气,应选用的试剂为___(填字母代号)。
A.浓氨水 B.浓硫酸 C.硝酸钾 D.生石灰 E.氢氧化钠
(3)根据实验要求,仪器连接的顺序为:a接___,___接___,___接___(用字母代号表示)。____________
(4)将氨气通入盛有氧化铜粉末的玻璃管中,加热有红色固体和无色气体单质生成。证明氨气具有______性,发生反应的化学方程式是________________。
(5)收集氨气,按下图所示玻璃装置进行实验。先打开旋塞①,B瓶中产生白色的烟,原因是_______________(用化学方程式表示);稳定后,关闭旋塞①,再打开旋塞②,B瓶中的现象是________________。
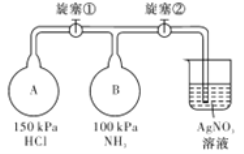
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】赫克反应(Heckreaction)在有机化学反应中有较广泛的应用,通式可表示为:R-X+R'-CH=CH2![]() R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)
R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)
已知A是最简单,最基本的芳香烃,现A、B、C、D等有机化合物有如下转化关系(部分反应物、生成物、反应条件已省略):
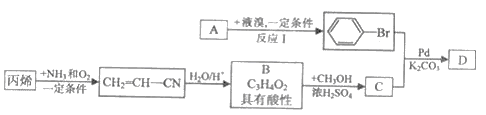
请回答下列问题。
(1)反应I的反应类型是______,化合物C的名称是______。
(2)写出B催化加氢反应的化学方程式__________。
(3)写出D的结构简式(不考虑立体异构):________________,生成D的反应中需要加入K2CO3而不是加入KOH,其目的是_______________。
(4)写出符合限定条件(既具有酸性又能使溴的四氯化碳溶液褪色)的C的同分异构体的结构简式(不考虑立体异构):_______________。
(5)苯甲酸苯甲酯既可以用作香料、食品添加剂及一些香料的溶剂,也可以用作塑料、涂料的增塑剂,还可以用来治疗疥疮。写出由A的最简单的同系物制备苯甲酸苯甲酯(![]() )的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为
)的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为 )__________________________
)__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的溶液中能大量共存的是( ) ①无色溶液中:K+、Cu2+、Na+、SO ![]()
②pH=11的溶液中:CO ![]() 、Na+、Cl﹣、NO
、Na+、Cl﹣、NO ![]()
③加入Mg能放出H2的溶液中:Cl﹣、HCO ![]() 、NO
、NO ![]() 、NH4+
、NH4+
④在由水电离出的c(OH﹣)=10﹣13 molL﹣1的溶液中:Na+、Ba2+、Cl﹣、I﹣
⑤能使红色石蕊试纸变为蓝色的溶液:Na+、Cl﹣、S2﹣、ClO﹣
⑥强酸性溶液中:Fe2+、Al3+、NO ![]() 、Cl﹣ .
、Cl﹣ .
A.①②⑤
B.②④⑥
C.②④
D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com