
 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )| A. | b电极反应式为O2+2H2O+4e-=4OH- | |
| B. | 电解时,a电极反应为:2Cl--2e-=Cl2↑ | |
| C. | 电解时,电子流动路径是:负极→外电路→b→溶液→a→正极 | |
| D. | 忽略能量消耗,当电池中消耗0.02gH2时,b极周围会产生0.02gH2 |
分析 左边装置是氢氧燃料电池,投放燃料的电极为负极,负极氢气失电子发生氧化反应,投放氧气的电极为正极,正极上氧气得电子发生还原反应,由于电解质溶液呈酸性,正极反应为:O2+4e-+4H+=2H2O;氢氧燃料电池作外接电源,电解卤水,连接负极的b电极是阴极,连接正极的a电极是阳极,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,据此分析解答.
解答 解:A.氢氧燃料电池中,正极上放电的是氧气,在酸性电解质环境下,电极反应式为:O2+4H++4e-═2H2O,故A错误;
B.还原性强的离子在阳极先放电,因为还原性:Br->Cl-,所以电解时a电极周围首先放电的是Br-而不是Cl-,电极反应为:2Br--2e-=Br2↑,故B错误;
C.电子在导线中移动,不能在溶液中移动,则电子流动路径是:负极→外电路→阴,阳极→正极,故C错误;
D.燃料电池和电解池中转移的电子数是相等的,当电池中消耗0.02gH2,根据电极反应H2-2e-=2H+可知转移电子0.02mol,b极的电极反应为:2H++2e-=H2↑,转移电子0.02mol,会产生0.02gH2,故D正确;
故选D.
点评 本题考查了原电池和电解池的工作原理,为高频考点,明确离子的放电顺序是解题关键,易错选项是C,注意电子不进入电解质溶液,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 136C与157N具有相同的中子数 | B. | 136C与C60是同位素 | ||
| C. | 157N与147N为同位素 | D. | 157N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | Fe2O3 | Al | 稀盐酸 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能发生丁达尔效应的分散系有氯化钠溶液、水等 | |
| B. | 电泳现象证明胶体是带电的 | |
| C. | 不能用过滤的方法除去氢氧化铁胶体中的可溶性杂质 | |
| D. | 将饱和FeCl3溶液加热至沸腾,可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  表示燃料燃烧反应的能量变化 | |
| B. | 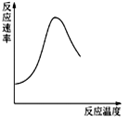 表示酶催化反应的反应速率随反应温度的变化 | |
| C. |  表示可逆反应从加入反应物开始建立化学平衡的过程 | |
| D. | 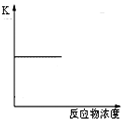 表示可逆反应的平衡常数随反应物浓度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a-2}^{a+b-2}$R | C. | ${\;}_{a+2}^{a+b+2}$R | D. | ${\;}_{a-2}^{a+b}$R |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com