
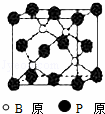
磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
回答下列问题:
(1)上述反应物中含有一种元素,其基态原子具有八种不同能量电子,写出其基态原子的价电子轨道表示式.
(2)BP中每个B或P原子均形成4个共价键,其中有一个配位键,提供空轨道是 原子.
(3)磷化硼的晶体类型是 ,B原子的杂化方式是 ,每生成1molBP,共形成 4 molB﹣P键.
(4)已知BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,判断电负性:P B (填“>”、“<”)
(5)BBr3分子中,B原子采取 杂化,键角为
(6)氮化硼晶体的熔点要比磷化硼晶体高,其原因是 .
考点:
晶胞的计算;原子核外电子排布;晶体的类型与物质熔点、硬度、导电性等的关系;原子轨道杂化方式及杂化类型判断.
专题:
原子组成与结构专题;化学键与晶体结构.
分析:
(1)其基态原子具有八种不同能量电子,该原子的能级有1S、2S、2P、3S、3P、3d、4S、4P,据此确定该元素;
(2)没有孤电子对的原子提供空轨道;
(3)根据其空间结构确定晶体类型,根据每个B原子含有的价层电子对个数确定杂化方式,根据每个B原子含有的B﹣P键个数计算;
(4)得电子能力越强的元素其电负性越强;
(5)根据电子对互斥理论确定其空间构型,根据空间构型确定键角;
(6)原子晶体中,物质熔点与原子半径、键长成反比.
解答:
解:(1)其基态原子具有八种不同能量电子,该原子的能级有1S、2S、2P、3S、3P、3d、4S、4P,所以该元素是第四周期的P区元素,为Br元素,其基态原子的价电子轨道表示式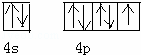 ,故答案为:
,故答案为: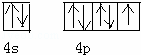 ;
;
(2)没有孤电子对的原子提供空轨道,B原子没有孤电子对,所以提供空轨道,P原子提供孤电子对,故答案为:B;
(3)根据其根据结构知,该物质为空间网状结构,所以是原子晶体,每个B原子含有4个σ键不含孤电子对,所以采取sp3杂化,每个B原子含有4个B﹣P键,所以每生成1molBP,共形成4molB﹣P键,故答案为:原子晶体,sp3;4;
(4)BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,则P元素得电子能力比B元素强,得电子能力越强的元素其电负性越强,所以电负性P>B,故答案为:>;
(5)BBr3分子中,B原子含有3个σ键不含孤电子对,所以采取sp2杂化,为平面三角形结构,键角是120℃,故答案为:sp2;120°;
(6)原子晶体中,物质熔点与原子半径、键长成反比,磷原子的半径比氮原子大,N﹣B共价键键长比B﹣P小,键能大,所以氮化硼晶体的熔点要比磷化硼晶体高,
故答案为:磷原子的半径比氮原子大,N﹣B共价键键长比B﹣P小,键能大.
点评:
本题考查了物质结构的综合性知识,原子的杂化方式、分子的空间构型、键角等知识点是高考的热点,应重点掌握.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
(Ⅰ). 某溶液可能含有Cl-、SO42-、CO32-、
NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红
褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的
沉淀。(已知Al(OH)3可被NaOH溶液溶解)由此可知原溶液中:
(1)至少存在  种离子
种离子
(2)Cl- 是 存在(填“一定”“一定不”“可能”),c(Cl‑)范围是 mol/L(若存在Cl- 则计算并填写,若不存在或可能存在Cl-,则此空不填)
(3)写出产生红褐色沉淀的离子方程式:
(Ⅱ).实验室要用98%(ρ=1.84 g·cm-3)的硫酸配制3.68 mol·L-1的硫酸溶液500mL
(1)计算所需98%的硫酸 mL。
(2)要配制3.68mol·L-1的硫酸溶液500mL,准确量取一定体积的98%的硫酸后,还需用到的实验仪器是(填写序号): .
①量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶 ⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将例所配制的硫酸溶液浓度偏低的是 。
A.浓硫酸溶解后未冷却,直接转移至容量瓶后定容
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外。
C.用量筒量取浓硫酸时,俯视读数
D.容量瓶使用前用含硫酸的溶液润洗了
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.(6分)实验室配制1mol/L Na2CO3溶液250mL。
(1)需要固体Na2CO3 g;
(2)该溶液中的阳离子数目为 个;
(3)需要物质的量浓度为5mol/L 的Na2CO3溶液 mL;
(4)将该溶液与足量稀硫酸反应,产生的气体在标准状况下的体积为 L。
(5)用固体Na2CO3配制该溶液的操作顺序是(用字母表示,不重复使用) 。
A.称量 B.洗涤 C.定容 D.溶解 E.摇匀 F.转移
(6)没有洗涤这步操作,所配制的溶液浓度 (填偏大、偏小或无影响)
Ⅱ.(4分) 在25℃、101kPa条件下,将15L O2通往10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气体中,V(CO)= L,V(H2)= L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中,V(CO): V(H2)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于几种分子中的化学键描述不正确的是( )
|
| A. | 苯每个碳原子的未参加杂化的2p轨道形成大π键 |
|
| B. | CH4中的4个C﹣H键都是H的1s轨道与C的2p轨道形成的s﹣p σ键 |
|
| C. | C2H4中,每个碳原子的sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
|
| D. | H2分子中存在s﹣s σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
以下四种物质,其中A、B各代表一种离子晶体的晶胞,C代表一种合金的晶胞,D则代表一个由A、B原子组成的团簇分子,其中化学式错误的是( )
|
| A. |
AB | B. |
XY3Z | C. |
EF | D. |
AB |
查看答案和解析>>
科目:高中化学 来源: 题型:
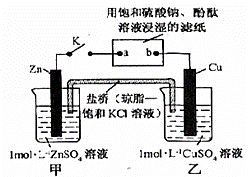
将右图所示实验装置,下列判断正确的是( )
|
| A. | 电子沿Zn→a→b→Cu路径流动 |
|
| B. | 铜电极上发生氧化反应 |
|
| C. | 盐桥中的K+向甲烧杯移动 |
|
| D. | 片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列五种烃①2﹣甲基丁烷②2,2﹣二甲基丙烷③戊烷④丙烷⑤丁烷,按沸点由高到低的顺序排列的是( )
A. ①>②>③>④>⑤ B. ②>③>⑤>④>① C. ③>①>②>⑤>④ D. ④>⑤>②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化合物.
已知:乙酸酐用AS表示,其结构式为
 +AS
+AS
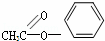 +CH2COOH
+CH2COOH

(1)C中含有官能团的名称为 .
(2)写出反应⑦的化学方程式 .
(3)写出G的结构简式 .
(4)任意写出一种符合下列条件的B的同分异构体
(a)苯环上只有两个取代基
(b)能发生银镜反应
(c)苯环上的一溴代物有两种
(d)加入NaHCO3溶液能产生使澄清石灰水变浑浊的气体
(5)写出反应类型:① ④ .
(6)下列可检验阿司匹林样品中混有水杨酸的试剂是 .
A.三氯化铁溶液 B.碳酸氢钠溶液 C.石蕊试液.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com