
����Ŀ������ʯ(Na3AlF6)����ˮ������ʯ��Ҫ����ұ�������������ۼ���Ҳ������ũ����ɱ������������ɫ�������´ɵ��ڹ���ȡ���ҵ����өʯ(CaF2����Ϊ96%)����������Ϊԭ�ϣ����÷������Ʒ��Ʊ�����ʯ���乤���������£�
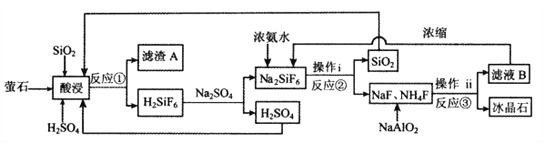
��1��Na3AlF6��Al�Ļ��ϼ�Ϊ__________������A����Ҫ�ɷ���__________(�ѧʽ)��
��2��Ϊ����߽����ʣ����������ʱ�ɲ�ȡ�Ĵ�ʩ�У����ʵ������¶ȣ��ڽ��裻��__________��
��3�������±����ݣ�ѡ���������ʱ���ʺϵ�����Ϊ__________��
ʵ���� | өʯƷλ | ����Ũ�� | ��Ӧ�¶�/�� | ���Na2SiF6������/g |
1 | 96% | 25% | 60-70 | 120 |
2 | 96% | 35% | 60-70 | 153 |
3 | 96% | 35% | 80-90 | 100 |
4 | 96% | 40% | 60-70 | 141 |
��4��д����Ӧ�۵Ļ�ѧ����ʽ__________��
��5���������Al2O3ұ��������ѧ����ʽΪ![]() ����ͼ��ʾһ��������Al2O3��Na3AlF6�����������ȹ����У�ij����y��ʱ��ı仯���ơ��������ʾ����__________��
����ͼ��ʾһ��������Al2O3��Na3AlF6�����������ȹ����У�ij����y��ʱ��ı仯���ơ��������ʾ����__________��
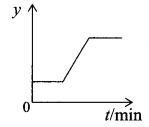
A.����O2������ B.������Na3AlF6������
C.��������Ԫ�ص����� D.��������Ԫ�ص���������
��6�����������յ��ŵ�Ϊ__________(��һ������)��
���𰸡� +3 CaSO4 �۴��ʯ������Ӧ��Ӵ���������ʵ����H2SO4��Ũ��(������������Ĵ𰸾���) 35%��H2SO4���Ʒ�Ӧ�¶���60-70��֮�� 2NaF+4NH4F+NaAlO2+2H2O=Na2AlF6+4NH3��H2O��2NaF+4NH4F+NaAlO2=Na3AlF6+4NH3+2H2O D ԭ�Ͽ���ѭ��ʹ����ԭ�������ʸߣ���Լԭ�������������豸��Ҫ�����(������������Ĵ𰸾���)
����������1��Na3AlF6��Al�Ļ��ϼ�Ϊ+3������ͼʾ����Ӧ����CaF2��SiO2��H2SO4��Ӧ����H2SiF4��A��������A��CaSO4��
��2��Ϊ����߽����ʣ����������ʱ�ɲ�ȡ�Ĵ�ʩ�У��۴��ʯ������Ӧ��Ӵ���������ʵ����H2SO4��Ũ�ȵȣ�
��3�������Ŀ������õ������H2SiF4�����ݱ���ʵ��2�л��Na2SiF6��������࣬ѡ���������ʱ���ʺϵ�����Ϊ35%��H2SO4���Ʒ�Ӧ�¶���60-70��֮����
��4����������ͼ����Ӧ���У�NaF��NH4F��NaAlO2����Na3AlF6��B��BӦ��NH3��H2O���ʷ�Ӧ�۵ķ���ʽ�ǣ�2NaF+4NH4F +NaAlO2+2H2O=Na2AlF6+4NH3��H2O��
��5��һ��������Al2O3��Na3AlF6�����������ȹ����У�A�����ڸ÷�Ӧ��Ӧ���ǹ��壬����O2�����ʲ��䣬A����B��������Na3AlF6�������ǽ������������۵㣬��δ���뷴Ӧ�������������䣬B����C���������Al2O3�õ��������ʹ�������Ԫ�ص�����Ӧ�ü��٣���C����D��һ��������Al2O3��Na3AlF6�����������ȹ����У�������ۻ������������������䣬���ŵ��Ľ��У�����������С����������Ԫ�ص��������䣬������������������������Ժ����������䣬�����������䣬���������������䣬��D��ȷ����ѡD��
��6����������ͼ�����������յ��ŵ�Ϊԭ�Ͽ���ѭ��ʹ����ԭ�������ʸߣ���Լԭ�������������豸��Ҫ��͡�


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݵ��飬���ʵļ�ͥװ�β��ϻ��ͷų��������������������к����ʣ�����һ���л�����ӵ����ģ����ͼ��ͼ�С���������������˫������������ͬ��С���������ͬԪ�ص�ԭ�ӣ�������Ԫ��λ�ڲ�ͬ�Ķ����ڣ�������ڸ��л������������ȷ���ǣ�������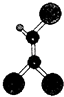
A.�л��ﻯѧʽΪC2HCl3
B.����������ԭ����ͬһ��ƽ����
C.���л���������ˮ
D.������Ȳ���Ȼ���ӳɵõ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]�л������C13H18O2����һ�����ϣ���ϳ�·����ͼ��ʾ������A����Է�������ͨ���������Ϊ56�����ĺ˴Ź���������ʾֻ������壻D���Է���������Ӧ���ڴ�������������1 mol D������2 mol H2��Ӧ���������ң����к���������CH3��
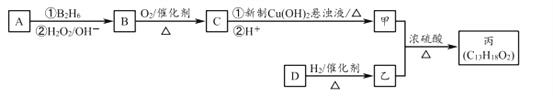
��֪��![]()
��1��D���������ŵ������� __________________��
��2���Ľṹ��ʽΪ________��C��ϵͳ����Ϊ________________��
��3��д����B����C�Ļ�ѧ����ʽ _____________________________________��
��4��д����FeCl3��Һ����ɫ�����һ�Ϊͬ���칹��������_______�֣����к˴Ź�������5��壬�ҷ����֮��Ϊ6��1��2��2��1�Ľṹ��ʽΪ_____________ ��
��5����֪�� ![]() ��д���Ա�ϩΪ�л�ԭ�ϣ��������Լ���ѡ���ϳ�
��д���Ա�ϩΪ�л�ԭ�ϣ��������Լ���ѡ���ϳ�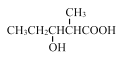 ��·��_______________________��
��·��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȼ�ϵ�ص��ܷ�Ӧ����ʽΪ2H2+O2=2H2O,�乤��ԭ����ͼ��ʾ���ش��������⣺
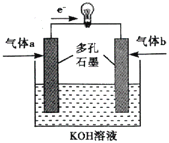
(1)��װ�ù��������У�������Ҫ������ת����ʽΪ__________��__________��
(2)�õ�ظ����ϵĵ缫��ӦʽΪ__________��
(3)����·��ͨ��0.2mol����ʱ,���ı�״���µ�����b�����Ϊ__________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ķе���ߵ���
A. ���� B. 2-������
C. 2-������ D. 2,2-��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�ĵ���ƽ�⣬����������ȷ����
A. ��ˮ���ȣ�pH����
B. ��ˮ�е���ϡ���ᣬc(H+)����
C. �����£���ˮ�м����������ᣬKw����
D. ��ˮ�м�����������粒��壬ˮ�ĵ���̶Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���в���ȷ���ǣ� ��
A.�ƺ�ˮ�ķ�Ӧ��þ���ҵĶ�
B.���ķǽ����Ա���ǿ
C.��������Ա�����ǿ
D.ˮ�����ȶ��ԱȰ�ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�����A��B�����2L���ܱ������У��������з�Ӧ��3A��g��+B��g��xC��g��+2D��g������2min����D��Ũ��Ϊ0.5mol/L��c��A����c��B��=3��5����C��ʾ��ƽ������v��C��=0.25molL��1min��1������˵����ȷ���ǣ� ��
A. �÷�Ӧ����ʽ�У�x=1
B. 2minʱ��A��ת����Ϊ50%
C. 2minʱ��A�����ʵ���Ϊ0.75mol
D. ��Ӧ����v��B��=0.25 molL��1min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CF2Cl2 ����Ʒ��Ϊ���ﰺ��12����������ȷ���ǣ� ��
A.����±����
B.������ͬ���칹��
C.����ԭ����ͬһƽ����
D.�ܷ�����ȥ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com