
| A. | 生铁 | B. | 铝热剂 | C. | 明矾 | D. | 赤铁矿 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2与CO2完全反应时转移电子数为2NA | |
| B. | 标准状况下11.2 L Cl2与4.25 g NH3所含有的原子数 | |
| C. | 标准状况下36 g H2O与1.204×1024个O2分子所占的体积 | |
| D. | 1mol固体NaHCO3所含有的阴阳离子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
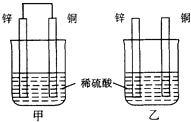
| A. | 两烧杯中铜片表面均有气泡产生 | B. | 甲中铜片是正极,锌片是负极 | ||
| C. | 两烧杯中溶液的pH均增大 | D. | 产生气泡的速度甲比乙快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量钠保存在汽油中 | |
| B. | 固态碘盛放在细口玻璃瓶中 | |
| C. | 液溴保存在加有少量水的盖有玻璃塞的棕色细口瓶中 | |
| D. | 浓硝酸盛放在盖有橡胶塞的棕色瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 不能发生银镜发应 | |
| B. | 1mol 该物质最多可与2molBr2反应 | |
| C. | 与NaHCO3、Na2CO3均能发生反应 | |
| D. | 1mol 该物质最多可与4mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al 和Mg | B. | K和 Na | C. | Na 和Al | D. | Zn 和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以上反应均可发生 | B. | 只有⑤不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有①不能发生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com