
分析 盐酸为一元酸,硫酸为二元酸,n(Ba(OH)2)是相等的,令n(Ba(OH)2)=1mol,计算需要盐酸、硫酸的物质的量,二种酸的浓度相等则其体积之比等于物质的量之比.
解答 解:相同体积、相同物质的量浓度的Ba(OH)2溶液溶质的物质的量相同,令n(Ba(OH)2)=1mol,
盐酸为一元酸,生成正盐消耗n(HCl)=2n(Ba(OH)2)=2mol,
硫酸为二元酸,生成正盐消耗n(硫酸)=n(Ba(OH)2)=1mol,二种酸的浓度相等则其体积之比等于物质的量之比,即2:1,故答案为:2:1.
点评 本题考查根据方程式的计算,难度不大,注意生成正盐时酸与氢氧化钡的物质的量关系.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过装有NaOH溶液的洗气瓶可除去二氧化碳中混有的HCl气体 | |
| B. | 向饱和的NaOH溶液中加入少量的Na2O固体后,恢复到原来的温度时,溶质的物质的量浓度增大 | |
| C. | 某无色溶液中加入BaCl2溶液,有白色沉淀生成,再滴入稀盐酸,沉淀不溶解,说明该溶液中一定含有SO42- | |
| D. | 回收KMnO4加热分解产生的MnO2,可用溶解→过滤→洗涤→干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正向移动 | B. | 逆向移动 | C. | 达到平衡 | D. | 不一定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
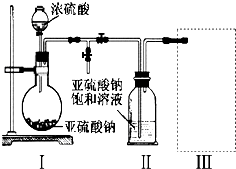


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com