
| 改变条件 | 移动方向 | c(OH-) | c(B+) |
| 升高温度 | | | |
| 降低温度 | | | |
| 加入BOH | | | |
| 加入大量H2O | | | |
| 加浓硫酸 | | | |
| 加NaOH | | | |
| 加BCl | | |


科目:高中化学 来源: 题型:
| A、分散系分为胶体和溶液 |
| B、电泳现象可证明胶体带电荷 |
| C、利用丁达尔效应可以区别溶液与胶体 |
| D、按照分散质和分散剂状态不同(固、液、气),它们之间可有6种组合方式 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
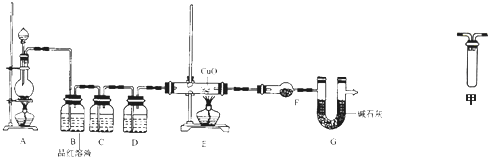
查看答案和解析>>
科目:高中化学 来源: 题型:

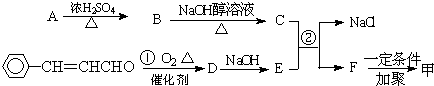

查看答案和解析>>
科目:高中化学 来源: 题型:
| OH- |
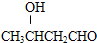
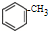
| KMnO4(H+) |
| △ |
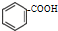
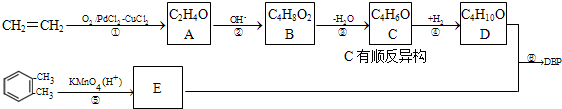
查看答案和解析>>
科目:高中化学 来源: 题型:
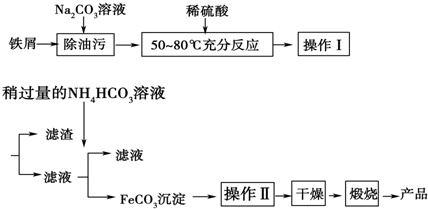

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com