
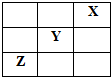
 X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答:
X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答: ;S能与Na形成化合物为Na2S,由钠离子与硫离子构成,电子式为,
;S能与Na形成化合物为Na2S,由钠离子与硫离子构成,电子式为, ,
, ;
; ;
;

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入醋酸钠,平衡向左移动 |
| B、加入碳酸钠,平衡向右移动 |
| C、加水稀释,C(H+)减小 |
| D、加水稀释,溶液中仅有的三种离子浓度都减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com