
(1)分析如图所示的三个装置,回答下列问题:

①装置a中铝电极上的电极反应式为________________________。
②装置b中产生气泡的电极为________电极(填“铁”或“铜”),装置c中铜电极上的电极反应式为_____________________________________。
燃料电池是一种高效低污染的新型电池。燃料电池所用燃料可以是氢气,也可以是其他燃料,如甲烷、肼等。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为:__________________。
②电池工作一段时间后电解质溶液的pH________(填“增大”“减小”或“不变”)。
(3)肼分子(H2N—NH2)可以在氧气中燃烧生成氮气和水,利用肼、氧气与KOH溶液组成碱性燃料电池,请写 出该电池反应的负极电极反应式______________________________。
出该电池反应的负极电极反应式______________________________。
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:2015-2016学年天津一中高一下期末化学试卷(解析版) 题型:选择题
氧化还原反应及盐与酸或碱的复分解反应遵循“强制弱”的规律,个别反应不符合该规律。下列反应中属于个别反应的是
A.2 Fe3++ Cu = 2Fe2+ + Cu2+
B.Cu2+ + H2S = CuS↓ + 2H+
C.Cl2 +2I- = 2Cl- + I2
D. Al3+ + 3NH3·H2O =Al(OH)3↓+ 3NH4+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁庄河高中高二下期末化学试卷(解析版) 题型:推断题
【化学——选修5:有机化学基础】龙葵醛(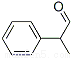 )是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。以下是以苯为原料生成龙葵醛的一种合成路线(部分反应条件及副产物已略去):
)是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。以下是以苯为原料生成龙葵醛的一种合成路线(部分反应条件及副产物已略去):
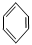
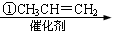
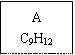

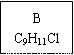

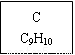
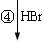
龙葵醛
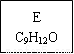

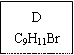
(1)龙葵醛的分子式为 ,其中含氧官能团的名称是 ;A物质得到的1H-NMR谱中有
个吸收峰,B的结构简式可能为 。
(2)反应③的反应类型为 ,反应⑤的反应条件为 。
(3)反应⑥的化学方程式为 。
(4)龙葵醛具有多种同分异构体,其中某些物质有下列特征:a.其水溶液遇FeCl3溶液呈紫色;b.苯环上的一溴代物有两种;c.分子中没有甲基。写出符合上述条件的物质可能的结构简式(只写两种):_________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁庄河高中高二下期末化学试卷(解析版) 题型:选择题
X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为( )
A.X>Y>Z>M B. X>Z>Y>M C. M>Z>X>Y D. X>Z>M>Y
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁庄河高中高二下期末化学试卷(解析版) 题型:选择题
NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.1mol FeI2与足量氯气反应时转移的电子数为2NA
B.2L 0.5mol•L﹣1硫酸钾溶液中阴离子所带电荷数为NA
C.1mol Na2O2固体中含离子总数为4NA
D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高一下期末化学试卷(解析版) 题型:选择题
金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2n H2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法正确的是
H2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法正确的是
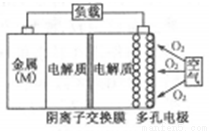
A.比较Mg、Al、Zn三种金属–空气电池,Mg–空气电池的理论比能量最高
B.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
C.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
D.在Mg–空气电池中,为防止负极区沉积Mg(OH)2,宜采用酸性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高一下期末化学试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高二下期末化学试卷(解析版) 题型:简答题
某废水中可能含有下列离子中的若干种:Fe3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-。现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅳ.向Ⅱ中所得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得滤液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成(提示:氢氧化铜可以溶解在过量的浓氨水中)。
请回答下列问题:
(1)该废水中一定含有的离子是____________,一定不含的离子是_________。
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是_____________________________。
(3)过滤除去Ⅳ中的蓝色沉淀,调 整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1∶4,其离子方程式为Al+NO3-
整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1∶4,其离子方程式为Al+NO3- +OH-→AlO2-+NH3+N2+H2O(未配平)。该反应中还原产物是___
+OH-→AlO2-+NH3+N2+H2O(未配平)。该反应中还原产物是___ _____。若除去0.2 mol NO3-,要消耗铝________g。
_____。若除去0.2 mol NO3-,要消耗铝________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com