
| A、2.3 g钠与97.7 g水反应后溶液中溶质的质量分数大于4% |
| B、钠跟CuSO4溶液反应生成的蓝色沉淀上有时会出现暗斑,这是因为析出了金属铜的缘故 |
| C、钠在化学反应中常常失去电子被氧化,做氧化剂,故Na+具有强氧化性 |
| D、钠、钾是低熔点的轻金属,所以钠、钾合金在常温时柔软似蜡 |


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、①③ | B、③② | C、③① | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、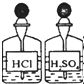 |
B、 |
C、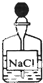 |
D、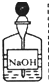 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色 |
| B、乙烯在一定条件下与水反应生成乙醇 |
| C、一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D、乙醇在浓硫酸的作用下,得到乙烯气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16g氧气和臭氧(O3)的混合气体所含原子数为NA |
| B、0.1molN5+离子中所含电子数为3.4NA |
| C、如果22.4 L的气体含有NA个分子,则必定是在标准状况下 |
| D、常温常压下,44gCO2中含有NA个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
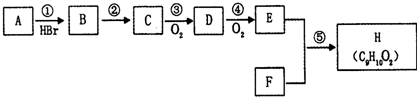
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com