
分析 (1)根据v=$\frac{△c}{△t}$计算化学反应速率;
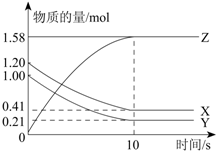
(2)X的物质的量浓度减少了$\frac{(1.2-0.41)mol}{1L}$=0.79mol/L;
(3)根据化学反应中各物质的物质的量变化量与化学计量数之比呈正比书写化学方程式.
解答 解:(1)反应开始到10s,用Z表示的反应速率为:v=$\frac{△c}{△t}$=$\frac{\frac{1.58mol}{1L}}{10s}$=0.158mol/(L•s),故答案为:0.158;
(2)X的物质的量浓度减少了$\frac{(1.2-0.41)mol}{1L}$=0.79mol/L,故答案为:0.79;
(3)由图象可以看出X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,化学反应中各物质的物质的量变化量与化学计量数之比呈正比,
则有Y:X:Z=(1.20mol-0.41mol):(1.0mol-0.21mol):1.58mol=1:1:2,10min达到平衡,则反应的化学方程式为X+Y?2Z,
故答案为:X+Y?2Z.
点评 本题考查物质的量随时间的变化曲线,以及化学平衡的计算,题目难度中等,注意把握化学方程式的判断方法.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
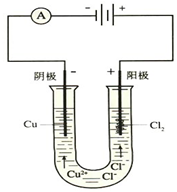 图为电解氯化铜溶液的装置
图为电解氯化铜溶液的装置 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 超导金属 | B. | 形状记忆金属 | C. | 储氢金属 | D. | 光纤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 五种元素中B元素的金属性最强 | |
| B. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| C. | 元素C、D、E的最高价氧化物对应水化物的酸性递减 | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
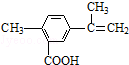
| A. | 在一定条件下,能发生取代、氧化、酯化和加聚反应 | |
| B. | 该物质分子中最多可以有11个碳原子在同一平面上 | |
| C. | 1 mol该物质最多可与4 mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗14mol氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com