


科目:高中化学 来源: 题型:
| A、可用碱式滴定管量取12.85 mL的KMnO4溶液 |
| B、测定氯水的pH,用干燥洁净的玻璃棒蘸取该溶液滴在湿润的pH试纸上 |
| C、反应物的总能量低于生成物的总能量时,一定不能自发进行反应 |
| D、由4P(s,红磷)═P4(s,白磷)△H=+139.2 kJ/mol,可知红磷比白磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| D |
| E |
| D |
| E |
查看答案和解析>>
科目:高中化学 来源: 题型:
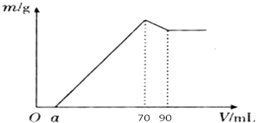 准确称取12g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol?L-1的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
准确称取12g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol?L-1的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
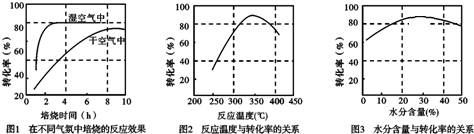
查看答案和解析>>
科目:高中化学 来源: 题型:
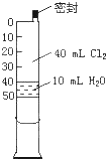 再吸进10mL水.
再吸进10mL水.查看答案和解析>>
科目:高中化学 来源: 题型:
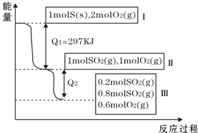 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示.已知:2SO2(g)+O2(g)?2SO3(g)△H=-96.6kJ?mol-1
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示.已知:2SO2(g)+O2(g)?2SO3(g)△H=-96.6kJ?mol-1查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别加热,观察是否有气体产生 |
| B、分别溶于水,加Ba(OH)2溶液观察是否有沉淀产生 |
| C、分别溶于水,滴加CaCl2溶液,观察是否有沉淀生成 |
| D、分别溶于水,通入CO2观察是否有NaHCO3产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com