
【题目】在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
(1)x值等于________________;
(2)A的转化率为 ;
(3)如果增大反应体系的压强,则平衡体系中C的质量分数 (增大、减小、不变)。
科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列叙述正确的有( )
A. 大米经蒸煮和发酵可酿造白酒 B. 油脂水解的最终产物为葡萄糖
C. 棉花和蚕丝的主要成分都是纤维素 D. 豆制品中的主要营养物质是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
②牙膏中其它成分遇到盐酸时无气体产生。
实验内容:Ⅰ.摩擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤,往滤渣中加入过量NaOH溶液。
(1)该过程涉及主要反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的沉淀质量,以确定碳酸钙的质量分数。
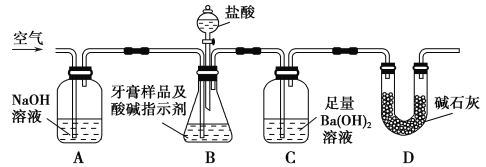
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________。
(3)C中反应生成沉淀的化学方程式是_____________________。
(4)下列各项措施中,能提高测定准确度的是________(填标号)。
a.滴加盐酸不宜过快
b.在A~B之间增添盛有浓硫酸的洗气装置
c.在加入盐酸之前,应排净装置内的CO2气体
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00 g样品三份,进行三次测定,测得C中产生沉淀平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(6)有人认为只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质溶液的燃料电池中发电,电池负极反应式为( )
A. H2-2e-=2H+ B. H2+2OH--2e-=2H2O
C. O2+4H++4e- =2H2O D. O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a,b,c,d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族,下列叙述正确的是
A.原子半径:d>c>b>a B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱 D.d单质的氧化性比a单质的氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验设计能达到实验目的的是
实验目的 | 实验设计 |
A.除去NaHCO3固体中的Na2CO3 将固体加热至恒重 B.制备无水AlCl3 蒸发Al与稀盐酸反应后的溶液 C.重结晶提纯苯甲酸 将粗品水溶、过滤、蒸发、结晶 D.鉴别NaBr和KI溶液 分别加新制氯水后,用CCl4萃取 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数纸盒为21。下列关系正确的是
W | X | |||
Y | Z |
A.氢化物沸点:W<Z B.氧化物对应水化物的酸性:Y>W
C.化合物熔点:Y2X3<YZ3 D.简单离子的半径:Y<X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53 kJ热量,则炭粉与氢气的物质的量之比为( )
A. 2∶3 B. 1∶2 C. 1∶1 D. 3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com