
【题目】某学生以铁丝和Cl2为原料进行下列三个实验.从分类角度分析,下列选项正确的是( ) 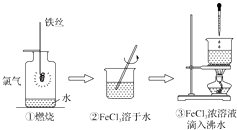
A.实验①、②所涉及的物质均为电解质
B.实验②、③均为放热反应实验
C.②、③均未发生氧化还原反应
D.实验①、③反应制得的物质均为纯净物
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】已知热化学方程式: H2O(g)=H2(g)+ ![]() O2(g);△H=+241.8kJ/mol
O2(g);△H=+241.8kJ/mol
H2(g)+ ![]() O2(g)=H2O(l);△H=﹣285.8kJ/mol
O2(g)=H2O(l);△H=﹣285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88 kJ
B.吸热44 kJ
C.放热44 kJ
D.吸热2.44 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、K+、Mg2+、Cu2+等阳离子及MnO﹣4、SiO2﹣4、AlO﹣2、CO2﹣3、HCO﹣3、SO2﹣4、Cl﹣等阴离子,已知:①该溶液呈无色②经测定溶液的pH=12③取少量溶液,加入稀盐酸[100mL、2molL﹣1]进行酸化,有白色沉淀生成,还得到一种无色无味的气体,该气体使澄清石灰水(足量)变浑浊.对酸化后的溶液过滤,得到滤液甲.
(1)由①、②、③可判断:原溶液中一定不存在的离子是 , 一定存在的离子是 .
(2)将滤液甲分成两等份,一份中逐滴加入氨水,最终有白色胶状沉淀,说明原溶液中一定有(填离子符号),刚开始加入氨水时,没有沉淀产生,原因是 . (用离子方程式表示);另一份中加入足量的Ba(NO3)2溶液,有白色沉淀生成,说明原溶液中一定有(填离子符号),过滤得到滤液乙.
(3)往滤液乙中加入足量的AgNO3溶液,过滤、洗涤、干燥得固体26.5g,则原溶液中是否有Cl﹣(填“是”或“否”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴单质具有广泛的工业价值,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性.某化学小组模拟工业流程从浓缩的海水中提取液溴,主要实验装置(夹持装置略去)及操作步骤如下: 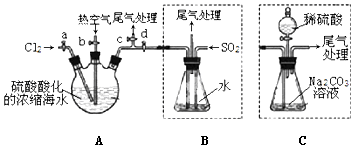
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴.
请回答:
(1)判断步骤①中反应已经结束的最简单方法为 .
(2)步骤②中鼓入热空气的作用为; 步骤③B中发生的主要反应的离子方程式为 .
(3)综合分析步骤①、②、③和④,这四步操作的最终目的为 .
(4)此实验中尾气可用(填选项字母)吸收处理. a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
(5)步骤⑤中,蒸馏用到的玻璃仪器除酒精灯、温度计、尾接管、锥形瓶外,还有和;要达到提纯溴的目的,操作中应控制的关键条件为 .
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴.滴加稀硫酸之前,C中反应生成了NaBr、NaBrO3等,该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验铵根离子的实验所依据的是:①氨气极易溶于水;②铵根离子与OH- 间发生反应产生氨气;③NH3·H2O电离出NH4+和OH -;④石蕊在碱性条件下变为蓝色。
A. ②④B. ①②③④C. ①②③D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知20℃时,饱和NaCl溶液的密度为ρg/cm3 , 物质的量浓度为c mol/L,则下列说法中不正确的是( )
A.温度低于20℃时,饱和NaCl溶液的浓度小于c mol/L
B.此溶液中NaCl的质量分数为 ![]()
C.20℃时,密度小于ρg/cm3的NaCl溶液是不饱和溶液
D.20℃时,饱和NaCl溶液的溶解度 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】14C是C的一种放射性核素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰击14N可使它转变为14C.下列说法正确的是
A. 14C原子最外层有6个电子B. 14C核素的中子数为8
C. 14C和14N互为同位素D. 14C16O2的质子数为46
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com