
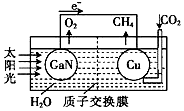
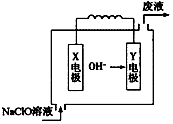
 科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.下列关于该电池叙述错误的是( )
科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.下列关于该电池叙述错误的是( )| A. | 为提高该人工光合系统的工作效率,可向装置中加入少量盐酸 | |
| B. | Cu电极上的电极反应为CO2+8e-+8H+=CH4+2H2O | |
| C. | H+从左池移向右池 | |
| D. | 当装置中有1mol CH4生成时,GaN电极有44.8LO2生成 |
分析 该装置中,根据电子流向知,GaN是负极、Cu是正极,负极反应式为:2H2O-4e-=4H++O2↑,正极反应式为:CO2+8e-+8H+=CH4+2H2O,电解质溶液中阳离子向正极移动,以此解答该题.
解答 解:A.向装置中加入少量盐酸,作电解质,增强导电性,则可以提高该人工光合系统的工作效率,故A正确;
B.根据电子流向知,Cu是正极,正极上二氧化碳得电子和氢离子反应生成甲烷,电极反应式为:CO2+8e-+8H+=CH4+2H2O,故B正确;
C.原电池工作时,阳离子向正极移动,则H+从左池移向右池,故C正确;
D.Cu是正极,电极反应式为:CO2+8e-+8H+=CH4+2H2O,GaN是负极,负极反应式为:2H2O-4e-=4H++O2↑,所以根据得失电子守恒,当装置中有1mol CH4生成时,GaN电极有标况下44.8LO2生成,未指明标况,无法计算,故D错误.
故选D.
点评 本题考查化学电源新型电池,题目难度中等,明确原电池原理为解答根据,注意正确判断电极反应、电子流向、离子流向,难点是电极反应式的书写.


科目:高中化学 来源: 题型:选择题
| A | B | C | D |
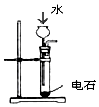 |  | 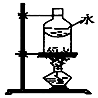 | 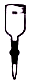 |
| 制乙炔的发生装置 | 蒸馏时的接收装置 | 分离固体氯化钠和碘单质 | 准确量取一定体积K2Cr2O7标准溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯酸甲酯和甲醇 | B. | 对硝基甲苯和含硝酸的水层 | ||
| C. | 硝酸钾和氯化钠 | D. | 氯化铵和碳酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知25℃时NH4CN溶液显碱性,则25℃时的电离常数K(NH3•H2O)>K(HCN) | |
| B. | 室温时,相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO2-4且浓度均为0.010 mol•L-1溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO2-4先产生沉淀 | |
| D. | 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地球上的绝大多数金属元素是以化合态形式存在 | |
| B. | 铜盐溶液都有毒,这主要是由于铜离子能使蛋白质变性 | |
| C. | 普通玻璃以纯碱、石灰石、石英砂为主要原料制得 | |
| D. | SO2气体通入氯水中可以增强氯水溶液的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 镁是一种重要的金属资源,在各领域都具有重要的作用.
镁是一种重要的金属资源,在各领域都具有重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为消除碘缺乏症,我国卫生部门规定食盐中必须加碘,其中碘元素以KI形式存在 | |
| B. | 空气污染日报中的空气污染指数的主要项目有可吸入颗粒物、二氧化硫、二氧化氮和二氧化碳 | |
| C. | 用含橙色的酸性重铬酸钾溶液的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| D. | 为了获得更好的消毒效果,医用酒精的浓度通常为95% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 温度(K) | 起始浓度(mol/L) | CH3OH的平衡浓度(mol/L) | ||
| H2 | CO | CH3OH | |||
| ① | 400 | 0.20 | 0.10 | 0 | 0.08 |
| ② | 400 | 0.40 | 0.20 | 0 | x |
| ③ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该反应的正反应是吸热反应 | |
| B. | X=0.16 | |
| C. | 平衡时,容器②中H2的体积分数比容器①的大 | |
| D. | 400K时若再向容器①中充入0.10molH2、0.10molCO和0.10molCH3OH,则平衡将向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷的3个碳原子不在同一直线上 | |
| B. | 丙烷可与氯水发生取代反应 | |
| C. | 丙烷能使溴水、酸性KMnO4溶液都褪色 | |
| D. | 丙烷可与强酸或强碱反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com