
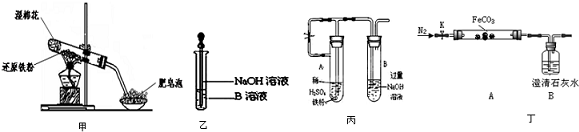
分析 本题以铁与水蒸汽反应为载体,探究反应后的固体成分,主要利用固体溶解后溶液里的Fe3+遇KSCN溶液显红色,Fe2+有还原性能使酸性KMnO4溶液褪色,遇NaOH溶液生成的白色沉淀遇空气立即变灰绿色最终变红褪色,因此制氢氧化亚铁时要隔绝空气,防氧化,还考查了Fe2+与HCO3-在溶液里会发生双水解反应;另外还探究了碳酸亚铁的热稳定性,利用在氮气的氛围里分解生成的气体能使石灰水变浑浊得出有二氧化碳气体生成,同时得到氧化亚铁,如果没有氮气保护将会氧气参与反应,得到的固体中有三价铁,据此作答;
(1)铁粉与水蒸气反应产物为四氧化三铁和氢气,产物四氧化三铁中有+2价的铁和+3价的铁,还有可能有过量的铁;过量的铁,可能将三价铁离子全部转化成二价铁离子;
(2)白色沉淀为氢氧化亚铁,红褐色沉淀为氢氧化铁,据此写出相应的化学反应方程式;
(3)Fe2+易被空气中的氧气氧化,具有还原性,Fe2+溶液易水解;
(4)硫酸亚铁易被氧化而变质,应排除溶液中的氧气,可用加热溶液的方法除去溶解氧;A管中产生的气体通入B管中排尽AB管中的空气,使AB充满还原性气体氢气,可防止生成的Fe (OH)2被氧化;试管B中为NaOH溶液,将A中液体压到B中与其反应;
(5)①Fe2+与HCO3-在溶液中发生反应生成的气体应为CO2,沉淀放置一段时间未见颜色变化,说明不是氢氧化亚铁沉淀,只能是碳酸亚铁沉淀,结合原子守恒和电荷守恒写出此反应的离子方程式;
②碳酸亚铁中二价铁有氧化性,加热前通氮气可将装置内的空气排尽,防止氧气氧化二价铁,二氧化碳能使澄清石灰水变浑浊;
③通入氮气,玻璃管内气压不会减小,所以不会产生倒吸现象;
④如果实验前不通入氮气,空气中的氧气会氧化二价铁,所得固体产物中会有三价铁,常见含三价铁的氧化物有氧化铁和四氧化三铁.
解答 解:(1)铁和水蒸气反应,产物为四氧化三铁和氢气,待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,一定发生Fe3O4+8H+=Fe2++2Fe3++4H2O,取少量溶液B滴加KSCN溶液,若溶液变红色Fe3++3SCN-?Fe(SCN)3,则说明所得溶液中存在的阳离子是一定有Fe3+,一定有Fe3O4,可能有过量的铁;若溶液未变红色,可能含有过量的铁,将三价铁离子全部转化成二价铁离子,Fe+2Fe3+═3Fe2+,
故答案为:A;C;
(2)可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,说明含有Fe2+离子,综上分析可知,白色沉淀为氢氧化亚铁,红褐色沉淀为氢氧化铁,所以反应为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)Fe2+溶液因为水解和还原性而不易保存,可以加入酸抑制其水解,加入还原性铁(铁钉)防止其被氧化,故答案为:还原;Fe2+易被空气中的氧气氧化而变质;铁粉;
(4)加热时气体的溶解度降低,所以,除去蒸馏水中溶解的O2常采用加热煮沸的方法;利用铁粉和稀硫酸反应产生的氢气排出试管A、B中的空气,使A、B充满还原性气体氢气,可排除试管中的氧气,防止Fe(OH)2 被空气中氧气氧化,一段时间后,关闭止水夹,试管A中生成的FeSO4溶液压到试管B,与试管B中的NaOH溶液反应,生成Fe(OH)2沉淀,在试管B中观察到白色的Fe(OH)2,
故答案为:把蒸馏水煮沸;利用铁粉和稀硫酸反应产生的氢气排出试管A、B中的空气,防止Fe(OH)2 被空气中氧气氧化;B.
(5)①硫酸亚铁溶液与碳酸氢铵溶液混合后生成二氧化碳气体和碳酸亚铁沉淀,发生反应的离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,故答案为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
②加热前利用氮气将空气排尽,防止空气中的氧气氧化固体中的二价铁,B中石灰水应变浑浊,说明有二氧化碳生成,故答案为:除去装置中的空气;分解产物有CO2;
③继续通入氮气,不会减小玻璃管内气压,所以不能产生倒吸,则不必拆开A、B之间橡胶管,故答案为:否;通入N2内压不会减小,不会倒吸;
④若不通入氮气直接加热分解,空气中的氧气会部分或全部氧化二价铁为三价铁,则分解的固体产物可能是FeO、Fe2O3或Fe3O4或Fe2O3和Fe3O4混合物,故答案为:FeO、Fe2O3;Fe3O4;Fe2O3和Fe3O4混合物;FeCO3(或FeO)被空气中的氧气氧化.
点评 本题主要考查了铁与水蒸气的反应以及产物的分析判断,考查了氢氧化亚铁的制备和碳酸亚铁的稳定性,掌握基础知识是解答的关键,本题难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 是一种非金属单质 | |
| B. | HD能在氯气中燃烧生成HCl和DCl气体 | |
| C. | 是一种化合物 | |
| D. | 在受热条件下,HD能还原氧化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 这是一个电解池 | |
| B. | C作阴极,Cu作阳极 | |
| C. | 电解的过程实际上是电解水 | |
| D. | 石墨电极上的反应是4OH--4e-=O2↑+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min Z的平均速率υ(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正) | |
| C. | 该温度下此反应的平衡常数K=1.44 | |
| D. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
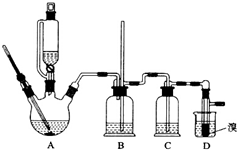 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
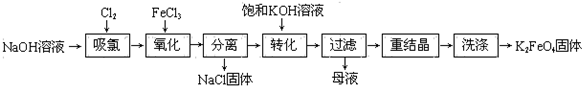
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯中的溶液没有恢复到室温就转移到容量瓶,一定会导致结果偏高 | |
| B. | 没有洗涤烧杯和玻璃棒,一定会导致结果偏低 | |
| C. | 容量瓶使用时没有干燥会导致结果偏低 | |
| D. | 使用量筒量取浓溶液后,没有把洗涤量筒得到洗涤液转移到容量瓶,会导致结果偏低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com