
| Zn的质量/g | Zn的形状 | 温度/℃ | 溶于酸的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 45 | 25 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 薄片 | 15 | 5 |
分析 (1)由表格中的数据可知,温度影响反应快慢,用表中数据画邮时间对温度的曲线图;
(2)当Zn的形状相同时,温度升高10℃,反应时间为原来的一半;
(3)B与F组温度相同,应是接触面积不同,反应速率不同.
解答 解:(1)A、B、C、D中Zn的形状相同,温度升高10℃,反应时间为原来的一半,用表中数据画出时间对温度的曲线图: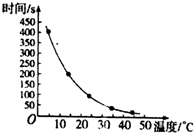 ,
,
故答案为: ;
;
(2)温度高,反应速率快,由数据可知,该反应温度升高10℃,化学反应速率加快到原来的2倍,
故答案为:反应温度升高10℃,化学反应速率加快到原来的2倍;
(3)B与F组温度相同,应是接触面积不同,反应速率不同,F组中锌应是粉末状,表面积较大,反应速率加快,
故答案为:F组中锌为粉末状,表面积较大,反应速率加快.
点评 本题考查影响化学反应速率的因素,注意控制变量及温度、接触面积的变化为解答的关系,把握常见影响因素即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 24Mg32S 晶体中电子总数与中子总数之比为1:1 | |
| B. | CO2和PCl5分子中各原子最外层都满足8 电子结构 | |
| C. | 若aXm+和bYn-两种离子电子层结构相同,则a-b=n-m | |
| D. | 元素周期表中第4 列元素形成的化合物数目最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把一段打磨过的镁条放入少量冷水中 | |
| B. | 把Cl2通入FeBr2溶液中 | |
| C. | 把绿豆大的钾投入水中 | |
| D. | 把溴水滴加到KI淀粉溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验过程 | 实验现象 |
| 实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④ | ①②无明显变化,③有气泡产生 |
| 实验2:分别将②、③、④取样于三支试管中,再分别加入溶液① | ③、④无明显变化,②溶液变红 |
| 实验3:分别向实验2的三支试管中,继续滴加入足量溶液④ | ④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
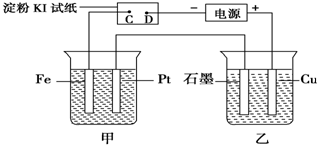
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
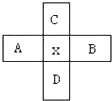 原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )
原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )| A. | 4x | B. | 4x+6 | C. | 4x+10 | D. | 4x+14 |
查看答案和解析>>
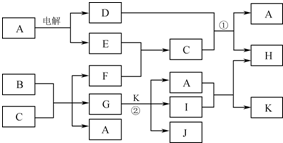
科目:高中化学 来源: 题型:推断题
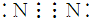 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
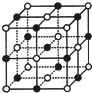 已知NiXO晶体晶胞结构为NaCl型(如图),由于晶体缺陷,x值小于1.测知NiXO晶体x=0.88,晶胞边长为4.28×10-10m 求:(已知:$\sqrt{2}$=1.4)
已知NiXO晶体晶胞结构为NaCl型(如图),由于晶体缺陷,x值小于1.测知NiXO晶体x=0.88,晶胞边长为4.28×10-10m 求:(已知:$\sqrt{2}$=1.4)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com