
分析 n(Al)=$\frac{2.7g}{27g/mol}$=0.1mol,n(HCl)=3mol/L×0.2L=0.6mol,根据2Al+6HCl=2AlCl3+3H2↑知,0.1molAl完全反应需要HCl0.3mol<0.6mol,所以HCl有剩余,n[Al(OH)3]=$\frac{3.9g}{78g/mol}$=0.05mol<0.1mol,有两种情况:1.加入的NaOH不足量,氯化铝有剩余;2.加入的NaOH不足量,氢氧化铝部分溶解,据此分析解答.
解答 解:n(Al)=$\frac{2.7g}{27g/mol}$=0.1mol,n(HCl)=3mol/L×0.2L=0.6mol,根据2Al+6HCl=2AlCl3+3H2↑知,0.1molAl完全反应需要HCl0.3mol<0.6mol,所以HCl有剩余,n[Al(OH)3]=$\frac{3.9g}{78g/mol}$=0.05mol<0.1mol,有两种情况:
1.加入的NaOH不足量,氯化铝有剩余,
根据NaOH+HCl=NaCl+H2O知,剩余0.3molHCl完全反应需要NaOH0.3mol;
根据AlCl3+3NaOH=Al(OH)3↓+3NaCl知,生成0.05molAl(OH)3需要n(NaOH)=3n[Al(OH)3]=3×0.05mol=0.15mol,
所以需要V(NaOH)=$\frac{0.3mol+0.15mol}{4mol/L}$=112.5mL;
2.加入的NaOH不足量,氢氧化铝部分溶解,
根据NaOH+HCl=NaCl+H2O知,剩余0.3molHCl完全反应需要NaOH0.3mol;
剩余0.05molAl(OH)3没有溶解,根据Al原子守恒知,有0.05molAl(OH)3溶解,
根据AlCl3+3NaOH=Al(OH)3↓+3NaCl知,生成0.1molAl(OH)3需要n(NaOH)=3n[AlCl3]=3×0.1mol=0.3mol,
根据Al(OH)3+NaOH=NaAlO2+2H2O知,0.05mol Al(OH)3溶解需要n(NaOH)=n[Al(OH)3]=0.05mol,
则需要V(NaOH)=$\frac{0.3mol+0.3mol+0.05mol}{4mol/L}$=162.5mL,
答:需要氢氧化钠体积为112.5mL或162.5mL.
点评 本题考查化学方程式有关计算,为高频考点,注意要进行过量计算,注意氢氧化铝能溶于氢氧化钠溶液,为易错题.


科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液和稀盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 碳酸钾溶液与稀硫酸反应:CO32-+H+═CO2↑+H2O | |
| C. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 实验室制取氧气:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2K++2Cl-+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )④
)④ ⑤葡萄糖⑥蛋白质.
⑤葡萄糖⑥蛋白质.| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2+2 HCL═Mg CL2+2 H2O | B. | 2 NaOH+H2SO4═Na2SO4+2 H2O | ||
| C. | Ba(OH)2+H2SO4═BaSO4+2 H2O | D. | 2 HCL+Cu(OH)2═CuCL2+2 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  点燃洒精灯 | B. |  称量10.05g固体 | C. | 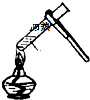 液体加热 | D. |  倾倒液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学利用下图装置,研究氯气的性质.请据图回答:
某同学利用下图装置,研究氯气的性质.请据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积均为22.4 L | B. | 具有相同的体积 | ||
| C. | 具有相同的质量 | D. | 具有相同的原子数目 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com