
A、Al2O3
| |||||
B、S
| |||||
C、Fe2O3
| |||||
D、MgCl2(aq)
|


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
A、氯原子的结构示意图: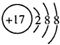 | ||
B、CO2分子的比例模型: | ||
C、具有10个中子的氧原子:
| ||
| D、乙烯的结构简式:C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子半径Z<M |
| B、Z位于元素周期表中第2周期、第ⅥA族 |
| C、X的最简单气态氢化物的热稳定性比Z的强 |
| D、Y的最高价氧化物对应水化物的酸性比X的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 物质 | X | Y | Z |
| 所含元素种数 | 1 | 2 | 3 |
| 分子中的电子总数 | 大于10 | 18 | |
| 燃烧热(kJ/mol) | -285.8 | -283 | -726.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
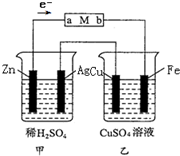 以下装置是某活动小组进行实验的装置图,回答下列问题.
以下装置是某活动小组进行实验的装置图,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
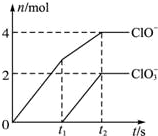 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2═5CaCl2+Ca(ClO3)2+6H2O.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2═5CaCl2+Ca(ClO3)2+6H2O.| c(ClO-) | ||
n(Cl
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )
一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )| A、20 s时,正反应速率大于逆反应速率 |
| B、10 s时,正、逆反应速率相等,达到平衡 |
| C、a曲线是NO2的物质的量随反应时间的变化曲线 |
| D、0~20 s内平均反应速率v(N2O5)=0.1 mol?(L?s)-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com