
【题目】下列分子中,所有原子的最外层均为8电子结构的是( )
A.BeCl2
B.H2S
C.NCl3
D.PCl5
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某盐酸的物质的量浓度。
(1)标准溶液应盛于___________(填“A”或“B”)滴定管中。
(2)若选用酚酞作指示剂,以0.1250 mol·L-1的标准氢氧化钠溶液滴定,如何判断滴定终点____________。
(3)实验数据记录如下表,请分析数据并计算,盐酸的物质的量浓度=_________mol·L-1。
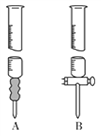
滴定次数 | 待测溶液体积/mL | ||
标准碱液 | |||
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.00 | 16.02 |
2 | 20.00 | 0.00 | 15.98 |
3 | 20.00 | 0.00 | 16.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。

已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是_________________(任写一种)。①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_________。
(3)步骤③中MnO2的其作用是__________________,另外一种物质X可以是__________。
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式__________。
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为__________________。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______。[已知:Ksp(MnS)=1.4×10―15]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通式为CnH2n-2的某烃在定容密闭容器中与足量O2完全燃烧,若反应前后压强不变(150℃),此烃分子式中n值为
A、2 B、3 C、4 D、5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学家在探索物质结构与性质方面做出了杰出贡献,发现元素周期律并绘制第一张元素周期表的化学家是( )
A.门捷列夫
B.汤姆生
C.卢瑟福
D.道尔顿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2![]() 2SO3,
2SO3,
△H<0。请回答下列问题:
(1)判断该反应达到平衡状态的标志是__________(填字母)。
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
(2)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的
是______________(填字母)。
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.降低温度
(3)将0.050 mol SO2 (g)和0.030 mol O2 (g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3) =0.040mol/L。计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程)。
①平衡常数K=______________;
②平衡时,SO2的转化率α (SO2) =_____________。
(4)SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3。己知NaHSO3溶液同时存在以下两种平衡:①HSO3-![]() SO32-+H+ ②HSO3-+H2O
SO32-+H+ ②HSO3-+H2O![]() H2SO3+OH-、常温下,0.1 mol/LNaHSO3溶液的 pH<7,则该溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
H2SO3+OH-、常温下,0.1 mol/LNaHSO3溶液的 pH<7,则该溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应A2+ B2![]() 2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是
2AB △H=QkJ/mol的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a、b为不同温度时的反应曲线(其他条件不变),c为在t3时刻开始缩小容器容积(温度不变)的变化曲线。下列有关说法正确的是
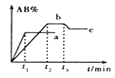
A. △H>0 B. AB一定是气体物质
C. 反应温度a低于b D. A2、B2中最少有一种是气态物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种金属,进行如下实验:①将A与B浸在稀硫酸中用导线相连,A逐渐溶解,B上有气泡逸出;②将A、D分别投入等浓度盐酸中,D比A反应剧烈;③将B浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C
C.D>B>A>C D.B>A>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含的杂质,选用的试剂正确的是
选项 | 物质(杂质) | 试剂 |
A | Al2O3(SiO2) | NaOH溶液 |
B | CO2(SO2) | Na2CO3溶液 |
C | NO(NO2) | 水 |
D | NaHCO3(Na2CO3) | Ca(OH)2溶液 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com