
【题目】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(气体体积已折算为标准状况下的体积)。下列分析正确的是( )
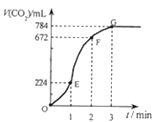
A. OE段表示的平均速率最快
B. EF段,用盐酸表示该反应的平均反应速率为 0.4mol/(L·min)
C. OE、EF、FG三段中,用二氧化碳表示该反应的平均反应速率之比为2:6:7
D. G点CO2不再增加的原因可能是盐酸已用完
【答案】BD
【解析】
A.曲线斜率表示化学反应速率快慢,斜率越大该阶段化学反应速率越大;
B.根据EF段生成二氧化碳的体积计算氯化氢的物质的量的变化量,进而计算氯化氢浓度变化,根据υ=△c/△t计算用盐酸表示该反应的平均反应速率;
C.各段终点与起点的纵坐标差值为各段生成的二氧化碳的体积,体积之比等于反应速率之比;
D.G点CO2不再增加的原因可能是盐酸浓度低,已用完。
A.斜率表示反应速率,斜率越大反应速率越大,由图可知,EF段斜率最大,所以EF段反应速率最大,故A错误;
B.由图可知EF段生成的二氧化碳的体积为672mL-224mL=448mL,所以二氧化碳的物质的量为0.448L÷22.4L·mol-1=0.02mol,根据CaCO3+2HCl═CaCl2+CO2↑+H2O,可知参加反应的氯化氢的物质的量为0.04mol,所以盐酸的浓度变化量为0.04mol÷0.1L=0.4mol·L-1,所以EF段用盐酸表示该反应的平均反应速率为0.4mol·L-1÷1min=0.4mol/(L·min),故B正确;
C.OE、EF、FG三段生成的二氧化碳体积分别为224mL、448mL、112mL,所以OE、EF、FG三段中,该反应用CO2表示的平均反应速率之比为224mL:448mL:112mL=2:4:1,故C错误;
D.G点表示收集的二氧化碳为从开始到G点生成的二氧化碳,总共784mL,G点CO2不再增加的原因可能是:盐酸浓度低,盐酸已经用完,故D正确;
故选BD。


科目:高中化学 来源: 题型:
【题目】如图是常见原电池装置,电流表A发生偏转。
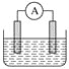
(1)若两个电极分别是锌、铜,电解质溶液是稀硫酸,正极的电极反应式为_________________;如果把电解质溶液换成硫酸铜溶液,则正极的电极反应式为____________________________。
(2)若电池的总反应是2FeCl3+Fe![]() 3FeCl2,则可以作负极材料的是________,负极反应式是____________________________,正极反应式是_________________________________。
3FeCl2,则可以作负极材料的是________,负极反应式是____________________________,正极反应式是_________________________________。
(3)若电解质溶液是稀硫酸,镁、铝两种金属作电极,则镁电极的反应式为_________________;若电解质溶液换作稀氢氧化钠溶液,镁、铝两金属作电极,则镁是________(选填“正极”或“负极”),总反应的离子方程式是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:

(1)常温下含碳量最高的气态烃是 (填字母).
(2)能够发生加成的烃有 种.
(3)一卤代物种类最多的是 (填写字母).
(4)写出实验室制D的化学方程式 .
(5)写出F发生硝化反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的叙述正确的是
A. 向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
B. 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
C. 在pH相同的盐酸和氯化铵溶液中水的电离程度相同
D. pH=11的NaOH溶液与pH=3醋酸溶液等体积混合,滴入石蕊溶液呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型锂空气二次电池放电情况如图所示,关于该电池的叙述正确的是 ( )
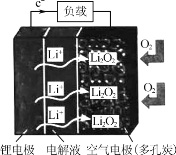
A. 电解液应选择可传递Li+的水溶液
B. 充电时,应将锂电极与电源负极相连
C. 放电时,空气电极上发生的电极反应为2Li++O2+2e-=Li2O2
D. 充电时,若电路中转移0.5 mol电子,空气电极的质量将减少3.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
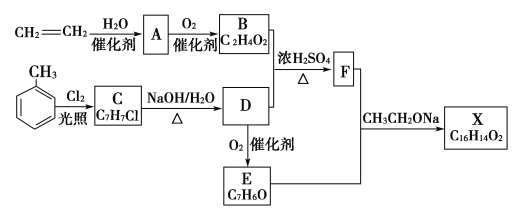
(1)写出由乙烯制取A的化学方程式:______________________________________________________。
(2)乙烯能使溴水和酸性KMnO4溶液褪色,二者褪色原理相同吗?________。原因是_____________________________________________________________________。
(3)以乙烯为原料,能否制得乙炔?________。若能,请写出相关的化学方程式:_________________________________________________________________________________。
(4)请写出C的含有苯环的同分异构体的结构简式:___________________________________。
(5)写出甲苯与浓硝酸和浓硫酸的混合酸反应的化学方程式:________________________。
(6)以甲苯为例说明有机物基团之间的相互影响:_______________________。
(7)写出C→D的化学方程式:__________________________________________,其反应类型为____________________________________。
(8)C能发生消去反应吗?________。原因是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某密闭容器中,可逆反应:A(g) + B(g)![]() xC(g)符合图中(Ⅰ)所示关系:
xC(g)符合图中(Ⅰ)所示关系:![]() (C)表示C气体在混合气体中的体积分数。由此判断,对图像 (Ⅱ) 说法不正确的是:
(C)表示C气体在混合气体中的体积分数。由此判断,对图像 (Ⅱ) 说法不正确的是:

A.p3>p4,Y轴表示A的转化率
B.p3>p4,Y轴表示B的质量分数
C.p3>p4,Y轴表示B的转化率
D.p3>p4,Y轴表示混合气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com