
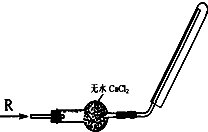
| A、NO | B、NO2 | C、H2 | D、Cl2 |
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
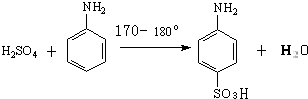
| 名称 | 性状 | 熔点/°C | 沸点/°C | 在水中的溶解度(g/100mL) |
| 苯胺 | 无色油状液体 | -6.1 | 184.4 | 3.6/18℃ |
| 对氨基苯磺酸 | 无色结晶 | 熔点365°C;内盐280~290°C | 0.8/10℃;1.08/20℃;6.67/100℃ | |

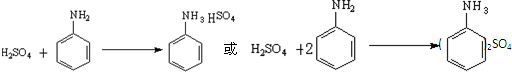

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届甘肃天水市一中高三第一次学段考试化学试卷(带解析) 题型:实验题
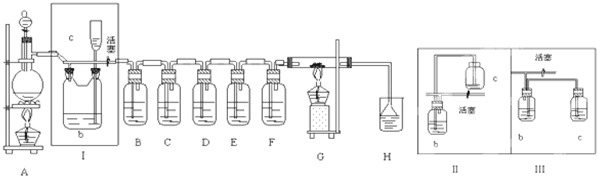
(14分) 如图所示是一个制取Cl2并以Cl2为原料进行特定反应的装置,其中各试剂瓶所装试剂为:B(Na2S)、C(FeBr2)、D(淀粉-KI)、E(SO2和BaCl2)、F(水)、H(紫色石蕊)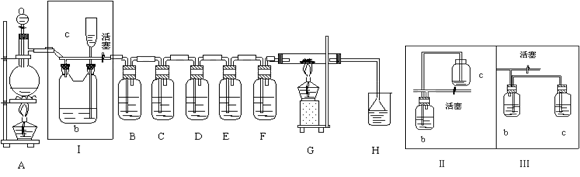
(1)写出实验室制取Cl2的化学方程式___________________________________________________________
(2)Ⅰ中b瓶内加入的液体是 。装置Ⅰ还可用右图中的装置_______(Ⅱ或Ⅲ)代替
(3)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让Cl2充满整个装置,再点燃G处酒精灯,回答下列问题:
①下列装置中的现象是B _________________;D _______________________ __
②写出E中反应的离子方程式:
_____________________________________;________________________________________
(4)G中硬质玻璃管内盛有碳粉,反应后的产物为CO2和HCl,写出G中的反应的化学方程式__________
(5)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是__________________________
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:实验题
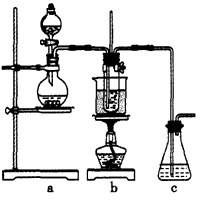
 5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________
5NaCl+NaClO3+3H2O,请推测在加热 NaClO溶液时发生反应的化学方程式:____________ 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com