
在一定温度下,可逆反应A(气)+3B(气)  2C(气)达到平衡的标志是
2C(气)达到平衡的标志是
A.A、B、C的分子数比为1:3:2 B.A、B、C的浓度相等
C.C生成的速率与C分解的速率相等
D.单位时间生成n mol A,同时生成3n mol B
科目:高中化学 来源: 题型:
 某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )
A.H2SO4浓度为4 mol·L-1
B.OA段产生的是NO,AB段的反应为
Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.混合酸中NO3-物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
现有等体积的Ba(OH)2、NaOH和NH3·H2O三种溶液,将它们分别与V1L、V2L、V3L等浓度的盐酸混合,下列说法中正确的是
A.若混合前三溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3
B.若混合前三溶液pH相等,酸碱恰好完全反应,则V1>V2>V3
C.若混合前三溶液物质的量浓度相等,酸碱恰好完全反应,则V1>V2>V3
D.若混合前三溶液pH相等,将它们同等倍数稀释后,则NaOH溶液pH最大
查看答案和解析>>
科目:高中化学 来源: 题型:
醇酸树脂是一种成膜性好的树脂,下面是一种醇酸树脂的合成线路:
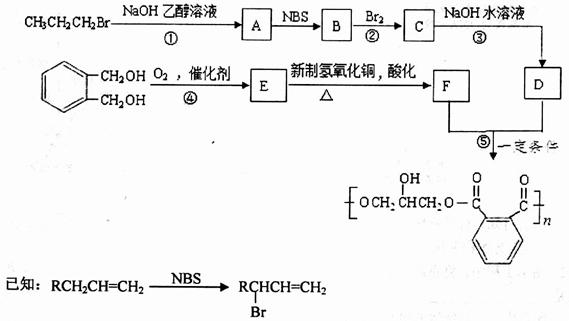
(1)B中含有的官能团的名称是_________________________。
(2)反应①、③的有机反应类型分别是___________________、____________________。
(3)下列说法正确的是__________(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2mol Ag
b.F能与NaHCO3反应产生CO2
c.检验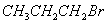 中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
 (4) _________________的同分异构体中同时符合下列条件的
(4) _________________的同分异构体中同时符合下列条件的
芳香族化合物共有__________种。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
(5)写出反应⑤的化学方程式________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
CH3COOH分别与CH3CH2OH和CH3CH218OH反应,生成的酯的相对分子质量关系
A.前者大于后者 B.前者小于后者 C.前者等于后者 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表中有机物的分子式排列规律,判断空格中物质的同分异构体数目是
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| CH4 | C2H4 | C3H8O | C5H10 | C6H14O | C7H16 | C8H16 | C9H20O |
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)===CO(g)+3H2(g)
ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)===CH3OH(g)
ΔH=-129.0 kJ/mol
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为_____。
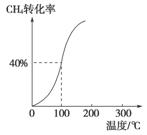
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________;
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将1.0 mol CO与2.0 mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的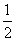 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
A.c(H2)减小
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加
D.重新平衡时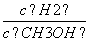 减小
减小
E.平衡常数K增大
(4)工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)CO(g)+2H2(g),此反应能自发进行的原因是:___。
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:
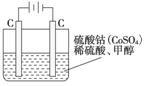
①写出阳极电极反应式_______________;
②写出除去甲醇的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种化合物,有的是药物,有的是香料。它们的结构简式如下所示:



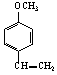
A B C D
(1)化合物A的分子式是子 ;A中含有的官能团的名称是 ;
(2)A、B、C、D四种化合物中互为同分异构体的是(填序号) ;
(3)化合物B的核磁共振氢谱中出现 组峰;
(4)1mol D最多能与 mol的氢气发生加成反应;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com