
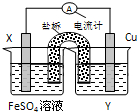
 依据氧化还原反应:Fe(s)+Cu2+(aq)=Fe2+(aq)+Cu(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:Fe(s)+Cu2+(aq)=Fe2+(aq)+Cu(s)设计的原电池如图所示.请回答下列问题:

科目:高中化学 来源: 题型:
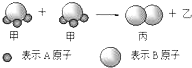
| A、1个乙分子中含有2个A原子 |
| B、该反应类型是分解反应 |
| C、Mr(甲)=Mr(乙)+Mr(丙) |
| D、该反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
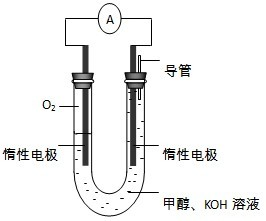 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
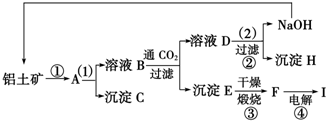 工业制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝.如图是从铝土矿中提纯Al2O3的简单示意图.其中涉及的一个反应是
工业制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝.如图是从铝土矿中提纯Al2O3的简单示意图.其中涉及的一个反应是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淡化海水,可向海水中加入净水剂明矾 |
| B、光导纤维属于有机合成新材料 |
| C、在电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
| D、食油在锅内过热着了火,熄灭它的最好方法是把油泼掉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com