

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

 WI2(g)”£ĪŖÄ£ÄāÉĻŹö·“Ó¦£¬×¼Č·³ĘČ”0.508gµā”¢0.736g½šŹōĪŁÖĆÓŚ50.0mLµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČČŹ¹Ęä·“Ó¦”£ČēĶ¼ŹĒWI2£Øg£©µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»Æ¹ŲĻµĶ¼Ļó£¬ĘäÖŠĒśĻßI£Ø0~t2Ź±¼ä¶Ī£©µÄ·“Ó¦ĪĀ¶ČĪŖT1£¬ĒśĻßII£Ø“Ót2æŖŹ¼£©µÄ·“Ó¦ĪĀ¶ČĪŖT2£¬ĒŅT2>T1”£Ōņ£ŗ¢ŁøĆ·“Ó¦µÄ”÷H 0£ØĢī”°“óÓŚ”±
WI2(g)”£ĪŖÄ£ÄāÉĻŹö·“Ó¦£¬×¼Č·³ĘČ”0.508gµā”¢0.736g½šŹōĪŁÖĆÓŚ50.0mLµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČČŹ¹Ęä·“Ó¦”£ČēĶ¼ŹĒWI2£Øg£©µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»Æ¹ŲĻµĶ¼Ļó£¬ĘäÖŠĒśĻßI£Ø0~t2Ź±¼ä¶Ī£©µÄ·“Ó¦ĪĀ¶ČĪŖT1£¬ĒśĻßII£Ø“Ót2æŖŹ¼£©µÄ·“Ó¦ĪĀ¶ČĪŖT2£¬ĒŅT2>T1”£Ōņ£ŗ¢ŁøĆ·“Ó¦µÄ”÷H 0£ØĢī”°“óÓŚ”±
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
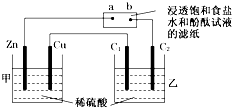
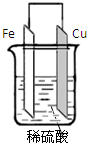
| A£®¼×³ŲÖŠ£¬Cu¼«ÉĻÓŠĘųÅŻ·Å³ö |
| B£®·¢ĻÖaµćø½½üĻŌŗģÉ« |
| C£®ŌŚC1”¢C2µē¼«ÉĻĖł²śÉśĘųĢåµÄĢå»ż±ČĪŖ2£ŗ1 |
| D£®ŅŅ³ŲČÜŅŗµÄpH¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
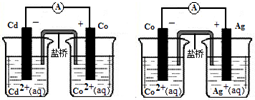
| A£®2Ag£Øs£©+Cd2+£Øaq£©=2Ag+£Øaq£©+Cd£Øs£© |
| B£®Co2+£Øaq£©+Cd£Øs£©=Co£Øs£©+Cd2+£Øaq£© |
| C£®2Ag+£Øaq£©+Cd£Øs£©=2Ag£Øs£©+Cd2+£Øaq£© |
| D£®2Ag+£Øaq£©+Co£Øs£©=2Ag£Øs£©+Co2+£Øaq£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
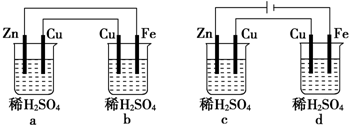
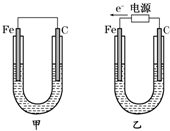
| A£®a”¢b¾łĪŖŌµē³Ų |
| B£®c”¢d¾łĪŖµē½ā³Ų |
| C£®b³ŲÖŠFe¼«·“Ó¦ĪŖFe-2e-ØTFe2+ |
| D£®d³ŲÖŠCu¼«·“Ó¦ĪŖ4OH--4e-ØTO2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com