
需要加入适当的氧化剂才能实现的反应
A.PCl3→PCl5 B.MnO4-→Mn2+ C.SO3→SO42- D.CO2→CO32-
科目:高中化学 来源:2016届山东省济宁市高一12月质检化学试卷(解析版) 题型:计算题
有铁和铝的混合物共5.5g,完全溶解于200mL 36.5%的浓盐酸(密度为1.2 g/mL)中,在标准状况下共收集到4.48L H2,求:
(1)浓盐酸的物质的量浓度为 。
(2)铁的质量为 ,铝的质量为 。
(3)将反应后剩余的溶液,用水稀释至500mL,求稀释后溶液中盐酸的物质的量浓度(HCl挥发忽略不计) 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省泰安市高一上学期期末考试化学试卷(解析版) 题型:选择题
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种。若该气体为无色气体,且通过品红溶液后,品红溶液褪色,剩余气体与空气接触时,很快变为红棕色。下列判断正确的是
A.肯定只有NO B.肯定有SO2和NO2
C.可能有Cl2和O2 D.肯定没有Cl2、O2和NO2
查看答案和解析>>
科目:高中化学 来源:2016届山东省高一上学期期中考试化学试卷(解析版) 题型:选择题
已知常温下在溶液中可发生如下两个离子反应:
Ge4++Fe2+=Fe3++Ge3+ ①;Sn2++2Fe3+=2Fe2++Sn4+ ②
由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序是
A.Sn2+、Fe2+、Ge3+ B.Sn2+、Ge3+、Fe2+
C.Ge3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ge3+
查看答案和解析>>
科目:高中化学 来源:2016届山东省高一上学期期中考试化学试卷(解析版) 题型:选择题
有甲、乙、丙三种溶液,进行如下操作:
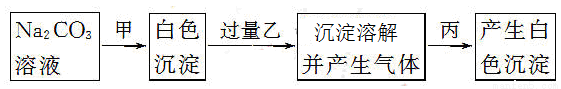
则甲、乙、丙三种溶液可能是
A.BaCl2、H2SO4、MgCl2 B.CaCl2、HNO3、BaCl2
C.CaCl2、HNO3、NaCl D.BaCl2、HCl、Na2SO4
查看答案和解析>>
科目:高中化学 来源:2016届山东省威海市高一上学期期末考试化学试卷(解析版) 题型:实验题
(1)某学生欲用11.9 mol·L-1的浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。该学生需要量取________mL浓盐酸进行配制。(保留小数点后1位)
(2)容量瓶是配制溶液的必需仪器。下列关于容量瓶及其使用方法的叙述,错误的是
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶长期贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
⑥容量瓶上标有的是温度 、容量 、刻度线
a.① ③ b.① ④ c.③ ⑤ d.⑤ ⑥
(3)① 该同学用配制的0.400 mol·L-1的盐酸,中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
② 假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
a.浓盐酸挥发,浓度不足
b.配制溶液时,未洗涤烧杯
c.配制溶液时,俯视容量瓶刻度线
d.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源:2016届山东省威海市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组中两种物质在溶液的反应,能用同一离子方程式表示的是
A.铁和稀盐酸、铁和稀硝酸
B.铜和浓硝酸、铜和稀硝酸
C.NaHCO3 + NaOH; NaHSO4 + NaOH
D.BaCl2 + H2SO4; Ba(OH)2 + Na2SO4
查看答案和解析>>
科目:高中化学 来源:2016届天津市五区县高一上学期期末考试化学试卷(解析版) 题型:填空题
食盐、碳酸钠和碳酸氢钠是生活中常见的钠盐。请回答下列问题。
(1)碳酸氢钠的水溶液显__________性。(填“酸”、“碱”或“中”)。除去碳酸钠固体中混有的少量碳酸氢钠,反应的化学方程式为_________________。
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2量,前者________后者(填“>”、“<”或“=”)。
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。试剂a、b分别是________(填序号)
A.Na2CO3 BaCl2 B.BaCl2 Na2CO3 C.BaCl2 Na2SO4
(4)工业上用电解饱和食盐水的方法生产氯气和烧碱。
①某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理_________________________________(用离子方程式表示)。
②工业上可用氨检验输送氯气的管道是否漏气。反应方程式如下:
 该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。
该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高一教学评估(一)化学试卷(解析版) 题型:选择题
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
A.灼热的铜丝在Cl2中剧烈地燃烧,产生棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.漂白粉是混合物,其有效成分是次氯酸钙
D.漂白粉放入稀盐酸中会降低漂白效果
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com