
分析 (1)钢铁发生吸氧腐蚀时,正极上氧气得电子发生还原反应、负极上铁失电子发生氧化反应;
(2)氢氧燃料酸性电池中,正极上氧气得电子和氢离子反应生成水,负极上氢气失电子生成氢离子.
解答 解:(1)钢铁发生吸氧腐蚀时,正极上氧气得电子发生还原反应,电极反应式为O2+4e-+2H2O═4OH-,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,故答案为:O2+4e-+2H2O═4OH-;Fe-2e-=Fe2+;
(2)氢氧燃料酸性电池中,正极上氧气得电子和氢离子反应生成水,负极上氢气失电子生成氢离子,正极反应式为O2+4H++4e-═2H2O,负极反应式为2H2-4e-═4H+;故答案为:O2+4H++4e-═2H2O;2H2-4e-═4H+.
点评 本题考查电极反应式的书写,明确各个电极上发生的反应是解本题关键,为高频考点,注意结合电解质溶液酸碱性书写,题目难度中等.


科目:高中化学 来源: 题型:解答题
 2-甲基-6-乙基壬烷
2-甲基-6-乙基壬烷 4,7,7-三甲基-1-辛烯
4,7,7-三甲基-1-辛烯查看答案和解析>>
科目:高中化学 来源: 题型:选择题
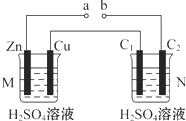
| A. | a、b连接,工作一段时间后装置M中溶液pH变大,装置N中溶液pH变小 | |
| B. | a、b连接,装置M中若有0.1 mol SO42-移到Cu电极,装置N中C2极放出H2 2.24 L(标准状况) | |
| C. | a、b未连接时,装置N中C1电极上有气体析出 | |
| D. | 不论a、b是否连接,装置M中观察到的实验现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HI、HBr、HCl、HF | B. | HCl、H2S、PH3、SiH4 | ||
| C. | H2O、H2S、HCl、HBr | D. | HF、H2O、PH3、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com