
| A. | CH2=CH-CH=CH2 | B. | 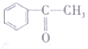 | C. | ClCH=CHCHO | D. | 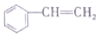 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断,注意结合信息中甲醛的平面结构.
解答 解:A、1,3-丁二烯含有2个碳碳双键,即具备2个烯烃的平面结构,所有原子可以共平面,故A不选;
B、分子中存在甲基,具有甲烷的四面体结构,所有原子不可能处于同一平面,故B选;
C、ClCH=CHCHO中含有烯烃结构,相当于-Cl和-CHO分别取代了乙烯中的2个H原子,且-CHO为平面结构,故所有原子可以共平面,故C不选;
D、苯为平面结构,乙烯为平面结构,通过旋转乙烯基连接苯环的单键,可以使两个平面共面,故苯乙烯中所有的原子可能处于同一平面,故D不选;
故选B.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,其中单键可以旋转.


科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水中:Ba2+、Fe2+、CO32- | |
| B. | 0.1 mol•L-1HNO3溶液中:Mg2+、SO42-、Cl- | |
| C. | 0.1 mol•L-1NH4Cl溶液中:K+、OH-、SO42- | |
| D. | 使石蕊变红色的溶液中:Na+、Cu2+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
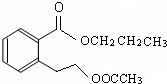 或
或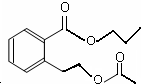 .
.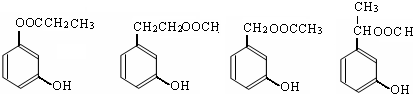 (任意两个).
(任意两个).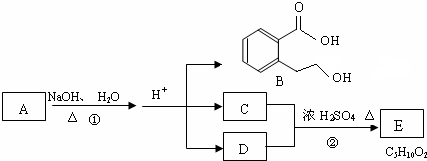
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
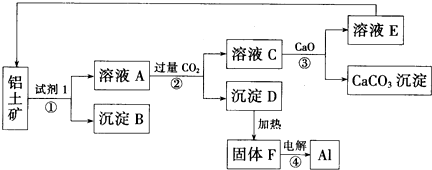
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 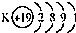 钾原子结构示意图 钾原子结构示意图 | |
| B. |  水合钠离子示意图 | |
| C. | 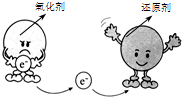 氧化还原反应与电子转移关系示意图 氧化还原反应与电子转移关系示意图 | |
| D. | 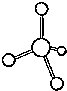 CH4分子示意图 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、陶瓷、水泥属于无机硅酸盐材料,其生产原料都是石灰石 | |
| B. | 钢铁里的铁和碳在潮湿的空气中因构成许多原电池而易发生电化学腐蚀 | |
| C. | 聚氯乙烯塑料在日常生活中可用来进行食品包装 | |
| D. | 铝制品在空气中不易被腐蚀,是因为常温下铝不与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
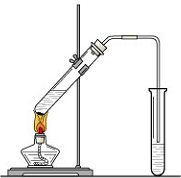 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置来制取乙酸乙酯.试回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置来制取乙酸乙酯.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成NH3的物质的量与消耗NH3的物质的量相等 | |
| B. | 消耗1molN2,同时消耗3molH2 | |
| C. | N2、H2、NH3在密闭容器中共存 | |
| D. | 正、逆反应速率都等于0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com