
| A、n(Fe)<n(S),总质量等于44g |
| B、n(Fe)>n(S),总质量等于44g |
| C、n(Fe)=n(S),总质量大于44g |
| D、n(Fe)<n(S),总质量大于44g |
| ||
| 11.2L |
| 22.4L/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、35Cl2与37Cl2互为同位素 |
B、 和 和 互为同分异构体 互为同分异构体 |
| C、与37Cl的得电子能力相同 |
| D、35Cl-和与它核外电子排布相同的微粒化学性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、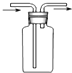 所示的气流方向可用于收集H2、NH3等 |
C、 所示装置,分离CCl4萃取I2水后的有机层和水层 |
D、 所示装置,可以证明氧化性:Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 实验 | 用CCl4提取溴水中的Br2 | 制取乙酸乙酯[来源:学优高考网] | 检验含有乙醇 蒸汽的乙烯 | 电石和饱和食盐水制取乙炔 |
| 装置或 仪器 |  |  |  |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 实验方案 |
| A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加少量AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色 |
| D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向AlCl3中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| B、硫酸氢钠溶液中加入足量的烧碱溶液:H++OH-=H2O |
| C、过氧化钠加入水:2Na2O2+2H2O=4OH-+O2↑+4Na+ |
| D、金属铝溶于氢氧化钠溶液:2Al+2OH-=2AlO2-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com