
向 ![]() 的平衡体系中加入H218O,过一段时间后18O是
的平衡体系中加入H218O,过一段时间后18O是
A.只存在于乙酸分子中 B.只存在于乙醇分子中
C.乙酸和乙酸乙酯分子中 D.乙醇、乙酸和乙酸乙酯分子中
科目:高中化学 来源: 题型:阅读理解
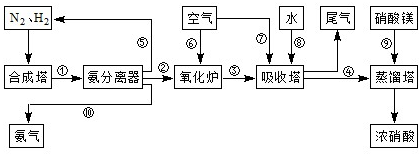
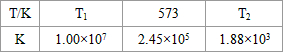
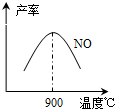 (3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1,不同温度下NO产率如右图所示.温度高于900℃时,NO产率下降的原因查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯水升高温度,电离平衡向正反应方向移动,Kw不变 | ||||
| B、在其它条件不变时,向H2(g)+I2(g)?2HI(g)平衡体系中加催化剂,反应速率加快,I2的转化率不变 | ||||
| C、pH=4的盐酸和氯化铵溶液分别加水稀释100倍,pH均变为6 | ||||
D、高铁电池:3Zn+2K2FeO4+8H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、该反应的平衡常数K=
| ||
| B、增大压强平衡右移,K平衡增大 | ||
| C、Y的平衡转化率是40% | ||
| D、其他条件不变,向平衡体系中加少量Z,v正、v逆均增大 |
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学选修5 3.3羧酸 酯练习卷(解析版) 题型:选择题
向酯化反应:CH3COOH+C2H5OH CH3COOC2H5+H2O的平衡体系中加
CH3COOC2H5+H2O的平衡体系中加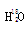 ,过一段时间,18O原子存在于( )
,过一段时间,18O原子存在于( )
A.只存在于乙醇分子中
B.存在于乙酸和H2O分子中
C.只存在于乙酸乙酯中
D.存在于乙醇和乙酸乙酯分子中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com