
【题目】下列有关铜与过量浓硫酸反应的实验说法不正确的是( )

A. 喷有碱液的棉花是为了防止SO2污染环境
B. 将水注入反应后冷却的试管a中,溶液变为蓝色
C. 铜片表面先发黑,反应完全后试管a底部有白色固体
D. 反应的化学方程式是Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
【答案】B
【解析】
A. 二氧化硫是有毒的大气污染物,二氧化硫有毒;
B. 浓硫酸具有吸水性;
C. 依据浓硫酸强氧化性和吸水性分析解答;
D. 铜与浓硫酸反应生成硫酸铜、二氧化硫和水;
A. 有碱液的棉花,防止二氧化硫散失到空气中,造成大气污染,其作用是吸收过量的SO2,防止环境污染,A项正确;
B. 浓硫酸具有吸水性,使生成的硫酸铜过饱和而析出白色的固体,B项错误;
C. 浓硫酸强氧化性,铜被氧化生成氧化铜,表面先发黑,浓硫酸具有吸水性,使生成的硫酸铜过饱和而析出白色的固体,C项正确;
D. 铜与浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,D项正确;
CuSO4+SO2↑+2H2O,D项正确;
答案选B。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 常温常压下,4.6 g NO2气体约含有1.806×1023个原子
B. 标准状况下,80 g SO3所占的体积约为22.4 L
C. 标准状况下,22.4 L CCl4中含有的CCl4分子数为NA
D. 标准状况下,22.4 L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种常用的抗组胺药物,一种合成路线如下:

已知:①C为最简单的芳香烃,且A、C互为同系物。
②2ROH+NH3![]() HNR2+2H2O(R代表烃基)。
HNR2+2H2O(R代表烃基)。
请回答下列问题:
(1)A的化学名称是___,H中的官能团名称是_______。
(2)由E生成F的反应类型是______,G的结构简式为______。
(3)A→B的化学方程式为_____。
(4)L是F的同分异构体,含有联苯(![]() )结构,遇FeCl3溶液显紫色,则L有___种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为_____。
)结构,遇FeCl3溶液显紫色,则L有___种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为_____。
(5)写出用氯乙烷和2-氯-1-丙醇为原料制备化合物![]() 的合成路线(其他无机试剂任选)。____
的合成路线(其他无机试剂任选)。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物R是合成某药物的中间体,结构简式为![]() 。下列说法正确的是
。下列说法正确的是
A.R与M( )互为同分异构体B.R中所有碳原子一定处于同一平面
)互为同分异构体B.R中所有碳原子一定处于同一平面
C.R的六元环上的一氯代物有4种D.R能发生取代反应、加成反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生用下图所示装置进行实验。以探究苯与溴发生反应的原理并分离提纯反应的产物。

请回答下列问题:
(1)写出装置Ⅱ中发生的主要化学反应方程式____________________________,其中冷凝管所起的作用为导气和________,Ⅳ中球形干燥管的作用是__________。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。Ⅲ中小试管内苯的作用是_________________________。
(3)能说明苯与液溴发生了取代反应的现象是______________________。
(4)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中以除去装置Ⅱ中残余的HBr气体。简述如何实现这一操作:______________________________________。
(5)纯净的溴苯是无色油状的液体,这个装置制得的溴苯呈红棕色,原因是里面混有______________,将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。①用蒸馏水洗涤,振荡,分液;②用__________洗涤,振荡,分液;③蒸馏。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于四个“封管实验”![]() 夹持装置未画出、
夹持装置未画出、![]() 固体易升华
固体易升华![]() 的说法正确的是
的说法正确的是
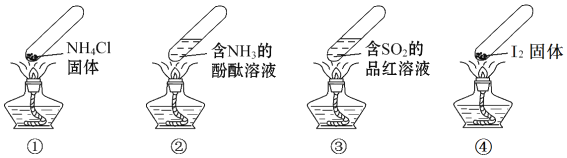
A. 加热时,![]() 中封管内固体消失
中封管内固体消失
B. 加热时,![]() 中溶液变红,冷却后又变为无色
中溶液变红,冷却后又变为无色
C. 加热时,![]() 中溶液变红,冷却后红色褪去,体现
中溶液变红,冷却后红色褪去,体现![]() 的漂白性
的漂白性
D. 加热又冷却的过程中,![]() 属于物理变化,
属于物理变化,![]() 属于化学变化
属于化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可用![]() 代替
代替![]() 制备
制备![]() ,反应后
,反应后![]() 元素以
元素以![]() 的形式存在。下列叙述不正确的是( )
的形式存在。下列叙述不正确的是( )
A.每生成1摩尔氯气,消耗1摩尔![]()
B.该反应中氧化性:![]()
C.参加反应的![]() 只有一部分被
只有一部分被![]() 氧化
氧化
D.用![]() 与
与![]() 制备相同量的氯气,参与反应的
制备相同量的氯气,参与反应的![]() 物质的量一样多
物质的量一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )

A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.NO和O2必须在催化剂表面才能反应
D.催化转化总化学方程式为2NO+O2+4CO 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种重要的化学原料,在生产和生活中应用十分广泛。
是一种重要的化学原料,在生产和生活中应用十分广泛。
(1)氯水中![]() 具有漂白性,能杀菌消毒。其电子式为_____________。
具有漂白性,能杀菌消毒。其电子式为_____________。
(2)实验室可用![]() 和浓盐酸反应制取
和浓盐酸反应制取![]() ,反应的离子方程式是_________。
,反应的离子方程式是_________。
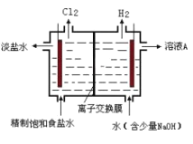
(3)工业上可采取电解饱和食盐水的方法制取![]() ,装置如图所示,图中的离子交换膜为_______(填“阳”或“阴”)离子交换膜。
,装置如图所示,图中的离子交换膜为_______(填“阳”或“阴”)离子交换膜。
(4)以![]() 为原料,用
为原料,用![]() 氧化制取
氧化制取![]() ,可提高效益,减少污染。反应如下:
,可提高效益,减少污染。反应如下:![]()
上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可使![]() 转化率接近100%,其基本原理如下图所示:
转化率接近100%,其基本原理如下图所示:
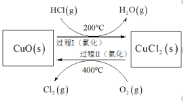
过程Ⅰ的反应为:![]()
![]()
①过程Ⅱ反应的热化学方程式为_______________。
②过程Ⅰ流出的气体通过稀![]() 溶液(含少量酚酞)进行检测,氯化初期主要为不含
溶液(含少量酚酞)进行检测,氯化初期主要为不含![]() 的气体,判断氯化结束时溶液的现象为___________。
的气体,判断氯化结束时溶液的现象为___________。
③相同条件下,若将氯化温度升高的300℃。溶液中出现上述现象的时间将缩短,其原因为______。
④实验测得在不同压强下,总反应的![]() 平衡转化率
平衡转化率![]() 随温度变化的曲线如图;
随温度变化的曲线如图;
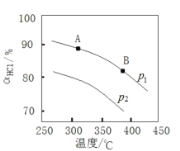
i 平衡常数比较:K(A)_________K(B)(填“>”“<”或“=”)。
ii 压强比较:p1_______p2 。(填“>”“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com