

分析 无色气体A与氧气连续反应得到C,且C为红棕色气体,则C为NO2,C与水反应生成D,A与氢气反应生成E,D与E反应生成F,而F与氢氧化钠反应可以得到E,D、E的水溶液酸碱性相反,E气体遇氯化氢气体会产生白烟,可推知A为N2、B为NO、D为HNO3、E为NH3、F为NH4NO3,据此解答.
解答 解:无色气体A与氧气连续反应得到C,且C为红棕色气体,则C为NO2,C与水反应生成D,A与氢气反应生成E,D与E反应生成F,而F与氢氧化钠反应可以得到E,D、E的水溶液酸碱性相反,E气体遇氯化氢气体会产生白烟,可推知A为N2、B为NO、D为HNO3、E为NH3、F为NH4NO3.
(1)由上述分析可知,E是NH3、C是NO2、A是N2、B是NO,
故答案为:NH3;NO2;N2;NO;
(2)D和E反应生成F的化学方程式:HNO3+NH3═NH4NO3,
故答案为:HNO3+NH3═NH4NO3;
(3)D的稀溶液与铜反应的化学方程式:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O.
点评 本题考查无机物推断,涉及氮元素单质化合物性质与转化,物质的颜色、反应现象及溶液酸碱性为推断突破口,难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 放电时,锂为负极,发生还原反应 | |
| B. | 充电时阳极反应式为:8Li2S-16e-═S8+16Li+ | |
| C. | 电解质可采用导电有机电解质 | |
| D. | 锂硫电池的理论电压为2.0V,则单位质量的单质硫的比能量为3.35 kW•h/kg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 丹参素在C上取代H的一氯代物有4种 | |
| B. | 在Ni催化下1mol丹参素最多可与4molH2加成 | |
| C. | 丹参素能发生取代、消去、中和、氧化等反应 | |
| D. | 1mol丹参素在一定条件下与足量金属钠反应可生成4molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
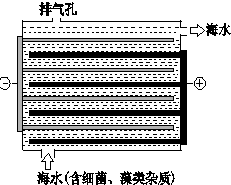 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.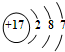 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 尿素CO(NH2)2 | B. | NH4NO3 | C. | NH4HCO3 | D. | (NH4)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
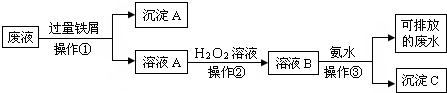
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaHCO3固体加入新制氯水,有无色气泡(H+) | |
| B. | 使红色布条褪色(Cl2) | |
| C. | 氯水能够导电(ClO) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1mol C12发生化学反应,转移的电子数一定为2NA | |
| D. | 在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的氮原子为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com