
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生。 |

(10分)(1)2H2O2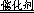 2H2O+O2↑(2分)
2H2O+O2↑(2分)
(2)研究温度对H2O2分解速率的影响(2分)
加快H2O2分解速率,使实验现象易于观察(2分)
(3)将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(2分)
(4)C点的即时速率(2分)
解析试题分析:(1)过氧化氢不稳定,容易分解生成水和氧气,则2H2O2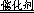 2H2O+O2↑;(2)实验①中过氧化氢的浓度和体积相同,氯化铁溶液的浓度和体积也相同,只有反应温度不同,分别是5℃、40℃,根据控制变量设计实验探究的规律,实验①的目的是研究温度对H2O2分解速率的影响;氯化铁溶液是双氧水分解反应的催化剂,实验中滴加氯化铁溶液的目的加快反应速率,,使实验现象易于观察;(3)实验②中过氧化氢溶液的体积相同,浓度不同,说明该实验的目的是研究浓度对双氧水分解速率的影响,因此其他条件相同即可,为了加快反应速率,便于观察实验现象,改进的方法可以是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率;(4)随着反应的进行,双氧水的物质的量逐渐减小,其浓度逐渐减小;减小反应物浓度,反应速率减小,则图中A、B、C点所表示的双氧水浓度大小关系为:A>B>C,因此三点表示的瞬时反应速率大小顺序是A>B>C,所以C点所表示的反应速率最慢。
2H2O+O2↑;(2)实验①中过氧化氢的浓度和体积相同,氯化铁溶液的浓度和体积也相同,只有反应温度不同,分别是5℃、40℃,根据控制变量设计实验探究的规律,实验①的目的是研究温度对H2O2分解速率的影响;氯化铁溶液是双氧水分解反应的催化剂,实验中滴加氯化铁溶液的目的加快反应速率,,使实验现象易于观察;(3)实验②中过氧化氢溶液的体积相同,浓度不同,说明该实验的目的是研究浓度对双氧水分解速率的影响,因此其他条件相同即可,为了加快反应速率,便于观察实验现象,改进的方法可以是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率;(4)随着反应的进行,双氧水的物质的量逐渐减小,其浓度逐渐减小;减小反应物浓度,反应速率减小,则图中A、B、C点所表示的双氧水浓度大小关系为:A>B>C,因此三点表示的瞬时反应速率大小顺序是A>B>C,所以C点所表示的反应速率最慢。
考点:考查探究实验,涉及过氧化氢分解反应的化学方程式、实验①的目的、滴加氯化铁溶液的目的、设计实验方案探究温度对过氧化氢分解速率的影响、设计实验方案探究浓度对过氧化氢分解速率的影响、化学反应速率图像、浓度对过氧化氢分解反应速率的影响规律的应用等。


 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:计算题
一定温度下的密闭容器中存在如下反应:CO(g)+H2O(g)  CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)达到平衡时,CO的转化率为多少?
(3)当CO的起始浓度仍为2mol·L-1,H2O(g)的起始浓度为6mol·L-1,求平衡时CO的转化率?
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
碘在科研与生活中有重要应用。某兴趣小组用0.50mol·L-1KI、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I-═2SO42-+I2(慢),I2+2S2O32-═S4O62-+2I- (快),
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变成为 色。为确保能观察到该现象,S2O32—与S2O82—初始的物质的量需满足的范围为:n(S2O32—):n(S2O82—) 。
(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表: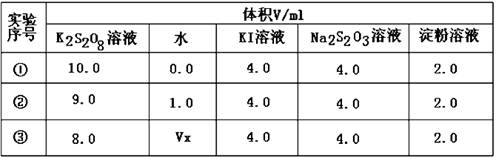
表中Vx= mL,反应速率最快的是 (填序号)。
(3)已知图中A曲线为某条件下,浓度c(S2O82—)~ 反应时间t的变化曲线图,若保持
其他条件不变, (填“B”或“C”)曲线为降低反应温度, (填“B”或“C”)曲线为加入催化剂。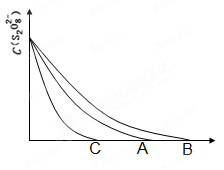
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数。反应的化学方程式: 2NH3(g)+CO2(g) NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:
(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图。
(2)制备氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。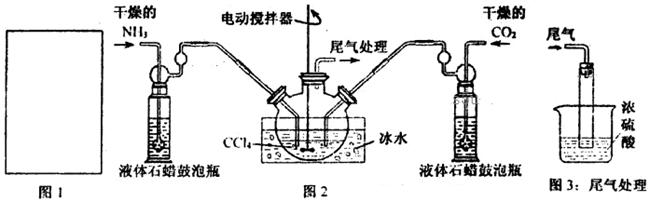
①从反应后的混合物中分离出产品的实验方法是_____________(填操作名称)。
②上图3中浓硫酸的作用是_______________________________________。
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积
忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
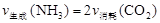
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤②中加热所用仪器的名称是___________________;
(2)步骤③中洗涤沉淀的操作是___________________________________。
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表: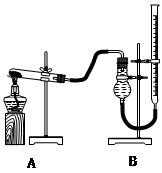
| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2 g | 无其他物质 | |
| ⑤ | 1.2 g | CuO 0.5 g | |
| ⑥ | 1.2 g | MnO2 0.5 g | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(15分) 某同学设计了如下图所示装置(部分夹持装置已略去),该装置可以用来进行多项
实验研究。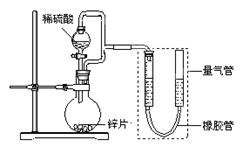
请回答:
(1)用上述装置探究影响化学反应速率的因素。
①圆底烧瓶中发生反应的离子方程式是 。
②用上述装置进行实验,以生成9.0 mL气体为计时终点,结果为t1>t2。
| 序号 | V(H2SO4)/mL | c(H2SO4)/mol·L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在25℃的条件下,下列叙述正确的是
A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO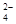 )= c(NH4+) )= c(NH4+) |
| B.pH=3的醋酸溶液,稀释至原体积的10倍后pH=4 |
| C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7 |
| D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-) 增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度时,向饱和的BaSO4溶液中加水,下列叙述正确的是
| A.BaSO4溶解度增大,Ksp不变 | B.BaSO4溶解度、Ksp均增大 |
| C.BaSO4溶解度不变,Ksp增大 | D.BaSO4溶解度、Ksp均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.常温下,某溶液中由水电离出的c(H+)=1×10-amo1·L–1,若a<7时,则该溶液可能为NaHSO4溶液 |
| B.常温下,中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸)=V(醋酸) |
| C.25℃时,已知Ka(CH3COOH)=1.7×10-5mo1·L–1、Ka(C6H5OH) =1.0×10-10mo1·L–1、 Ka1(H2CO3) = 4.2×10-7mo1·L–1 、Ka2(H2CO3) =5.6×10-11mo1·L–1pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| D.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加入稀盐酸有气泡产生,说明常温下Ksp(BaSO4)>Ksp(BaCO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com