
分析 (1)石灰水与二氧化碳反应生成碳酸钙;
(2)碘易溶于酒精;
(3)硫能与氢氧化钠反应生成硫化钠和亚硫酸钠;
(4)强碱和SiO2反应.
解答 解:(1)石灰水与二氧化碳反应生成碳酸钙,碳酸钙能与盐酸反应,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)碘易溶于酒精,因此能用酒精洗涤,故答案为:用酒精洗涤;
(3)硫能与氢氧化钠反应生成硫化钠和亚硫酸钠,离子方程式3S+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$2S2-+SO32-+3H2O:,故答案为:3S+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$2S2-+SO32-+3H2O;
(4)强碱和SiO2反应,无法用试剂复原得到光滑的玻璃,故答案为:玻璃瓶发“毛”是强碱和SiO2(玻璃中)反应之故,无法用试剂复原.
点评 本题考查仪器的洗涤、元素及其化合物的性质等知识,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | Al→Al2O3→Al(OH)3→NaAlO2 | B. | Fe→FeO→Fe(OH)2→Fe(OH)3 | ||
| C. | S→SO3→H2SO4→MgSO4 | D. | N2→NO→NO2→HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水和氯化亚铁溶液 | B. | 铁屑和氯化铜溶液 | ||
| C. | 铁屑和过量稀硫酸 | D. | 过量铁屑和氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器Ⅰ、Ⅱ中正反应速率不相同 | |
| B. | 容器Ⅰ中CO 的物质的量比容器Ⅱ中的多 | |
| C. | 容器I中反应的平衡常数小于Ⅲ中 | |
| D. | 容器Ⅲ中CO 的浓度比容器II中CO浓度的2倍还多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅熔点高硬度大,可用于制作光导纤维 | |
| B. | 氢氧化铝具有弱碱性,可用于胃酸中和剂 | |
| C. | 铁比铜活泼,氯化铁不能用于腐蚀铜板 | |
| D. | 氧化铁能与酸反应,可用于制作红色涂料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl溶液腐蚀印刷电路板Fe3++Cu═Fe2++Cu2+ | |
| B. | 少量CO2通入澄清石灰水中:CO2+Ca2++2OH-═CaCO3↓+H2O | |
| C. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
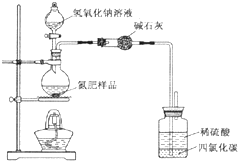 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:| 氢氧化钠溶液体积/mL | 40.00mL | ||
样品质量/g | 7.750 | 15.50 | 23.25 |
氨气质量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
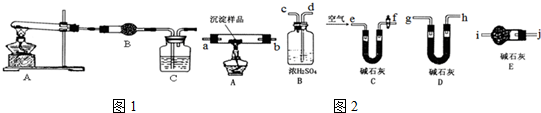
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com