
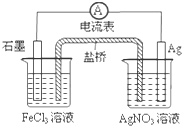
| A. | 导线上电子由Ag极流向石墨极 | B. | 负极电极反应式:Fe3++e-═Fe2+ | ||
| C. | 盐桥中阴离子移向AgNO3溶液 | D. | 总反应为:Fe3++Ag═Fe2++Ag+ |
分析 Ag失电子为原电池的负极,石墨为正极,正极发生Fe3++e-═Fe2+,负极发生Ag-e-=Ag+,原电池工作时,阳离子向正极移动,阴离子向负极移动,电子从负极应外电路流向正极,反应的总方程式为Fe3++Ag═Fe2++Ag+,以此解答该题
解答 解:A.在外电路中,电子从负极应外电路流向正极,即电子由Ag电极流向石墨电极,故A正确;
B.Ag失电子为原电池的负极,则负极电极反应式:Ag-e-=Ag+,故B错误;
C.阴离子向负极移动,盐桥中阴离子移向AgNO3溶液,故C正确;
D.正极发生Fe3++e-═Fe2+,负极发生Ag-e-=Ag+,总方程式为Fe3++Ag═Fe2++Ag+,故D正确.
故选:B.
点评 本题考查原电池知识,侧重于学生的分析能力和基本理论的理解和应用能力,难度不大,注意把握电极反应的判断和电极方程式的书写.


科目:高中化学 来源: 题型:解答题


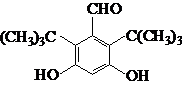
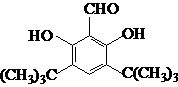
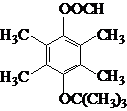 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
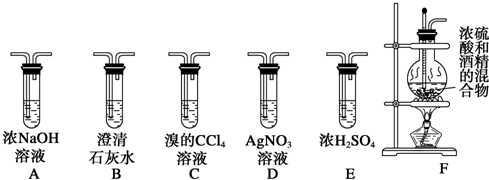
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
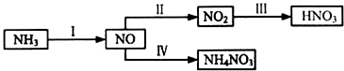
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | a | b | c |
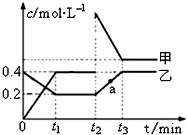
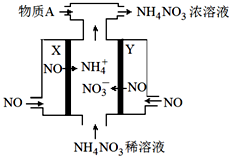
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
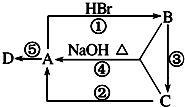 如图A、B、C是中学化学中最常见的三种有机化合物,D是高分子化合物,常用来制造食品和药品包装袋,试回答:
如图A、B、C是中学化学中最常见的三种有机化合物,D是高分子化合物,常用来制造食品和药品包装袋,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:1 | B. | 1:2:3 | C. | 3:1:1 | D. | 1:3:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 爆炸力极强的N5变成N2是化学变化 | |
| B. | 水晶、玛瑙、钻石的主要成分均为SiO2 | |
| C. | NaCl溶液和Fe(OH)3胶体可以用过滤的方法分离 | |
| D. | 向鸡蛋清溶液中加入(NH4)2SO4或CuSO4均有鸡蛋清析出,其原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com