
| A. | 在反应CaH2+2H2O═Ca(OH)2+2H2↑中,水作氧化剂 | |
| B. | 根据反应Cu+H2SO4$\frac{\underline{\;电解\;}}{\;}$CuSO4+H2↑可推出Cu的还原性比H2的强 | |
| C. | 反应3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是3:1 | |
| D. | 因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 |
分析 A.CaH2中H元素的化合价升高,水中H元素的化合价降低;
B.常温下Cu与稀硫酸不反应,不能利用电解反应判断;
C.NO2为氧化剂,也为还原剂,1mol氧化剂得到电子与2mol还原剂失去电子相等;
D.I2+2NaClO3═2NaIO3+Cl2中I元素的化合价升高,Cl元素的化合价降低.
解答 解:A.CaH2中H元素的化合价升高,水中H元素的化合价降低,则水为氧化剂,故A正确;
B.常温下Cu与稀硫酸不反应,不能利用电解反应判断,实际上Cu的还原性比H2的弱,故B错误;
C.NO2为氧化剂,也为还原剂,1mol氧化剂得到电子与2mol还原剂失去电子相等,则3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是1:2,故C错误;
D.I2+2NaClO3═2NaIO3+Cl2中I元素的化合价升高,Cl元素的化合价降低,置换反应I2+2NaClO3═2NaIO3+Cl2能发生,与Cl2的氧化性强于I2的氧化性不矛盾,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、氧化还原反应应用等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷能燃烧,乙烯不能 | |
| B. | 甲烷和乙烯都能使溴水褪色 | |
| C. | 甲烷和乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 甲烷和乙烯完全燃烧的产物都是CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| B. | 要鉴别己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| C. | 除去溴苯中少量的溴,可以加水后分液 | |
| D. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
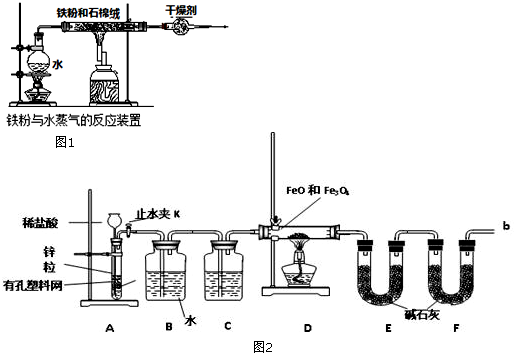
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每消耗1molCH4可以向外电路提供4mole- | |
| B. | 电池放电后,溶液PH不断升高 | |
| C. | 负极上O2得到电子,电极反应式为:O2+2H2O+4e-═4OH- | |
| D. | 负极上CH4失去电子,电极反应式:CH4+10OH--8e-═CO32-+7H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com