
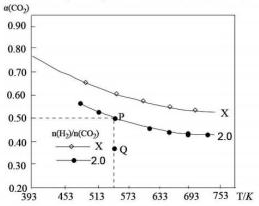
 在两个固定体积均为1L密闭容器中以不同的氢碳化比[n(H2):n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)△H.CO2的平衡转化率a(CO2)与温度的关系如图所示.下列说法正确的是( )
在两个固定体积均为1L密闭容器中以不同的氢碳化比[n(H2):n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)△H.CO2的平衡转化率a(CO2)与温度的关系如图所示.下列说法正确的是( )| A. | 该反应在高温下自发进行 | |
| B. | 氢碳比:X<2.0 | |
| C. | 若起始时,CO2、H2、浓度分分别为0.5mol/L和1.0mol/L,则可得P点,对应温度的平衡常数的值为512 | |
| D. | 向处于P点状态的容器中,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,再次平衡后a(CO2)减小 |
分析 A.根据△H-T△S<0反应自发进行分析;
B.氢碳比[$\frac{n({H}_{2})}{n(C{O}_{2})}$]越大,二氧化碳的转化率越大;
C.由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比[$\frac{n({H}_{2})}{n(C{O}_{2})}$]=2,起始时氢气为1mol/L、二氧化碳为0.5mol/L,则二氧化碳浓度变化量为0.25mol/L,则:
2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)
起始浓度(mol/L):0.5 1 0 0
变化浓度(mol/L):0.25 0.75 0.125 0.5
平衡浓度(mol/L):0.25 0.25 0.125 0.5
代入平衡常数表达式K=$\frac{c({C}_{2}{H}_{4})×{c}^{4}({H}_{2}O)}{{c}^{2}(C{O}_{2})×{c}^{6}({H}_{2})}$计算;
D.P点平衡时,CO2、H2、C2H4、H2O的浓度比值为2:2:1:4,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,增大了氢气的浓度平衡正向移动.
解答 解:A.由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,则正反应为放热反应,故△H<0,反应的熵变△S<0,若△H-T△S<0,则需在低温下进行,故A错误;
B.氢碳比[$\frac{n({H}_{2})}{n(C{O}_{2})}$]越大,二氧化碳的转化率越大,故氢碳比:X>2.0,故B错误;
C.由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比[$\frac{n({H}_{2})}{n(C{O}_{2})}$]=2,起始时氢气为1mol/L、二氧化碳为0.5mol/L,则二氧化碳浓度变化量为0.25mol/L,则:
2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)
起始浓度(mol/L):0.5 1 0 0
变化浓度(mol/L):0.25 0.75 0.125 0.5
平衡浓度(mol/L):0.25 0.25 0.125 0.5
代入平衡常数表达式K=$\frac{c({C}_{2}{H}_{4})×{c}^{4}({H}_{2}O)}{{c}^{2}(C{O}_{2})×{c}^{6}({H}_{2})}$=$\frac{0.{5}^{4}×0.125}{0.2{5}^{2}×0.2{5}^{6}}$=512,故C正确;
D.P点平衡时,CO2、H2、C2H4、H2O的浓度比值为2:2:1:4,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,增大了氢气的浓度平衡正向移动,二氧化碳的转化率增大,即再次平衡后a(CO2)增大,故D错误.
故选:C.
点评 本题考查化学平衡计算与影响因素、平衡常数、化学平衡图象等,侧重考查对图象的分析获取信息能力,难度中等,注意把握三段式在化学平衡计算中的应用方法,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有7个主族,7个副族,1个零族,1个Ⅷ族,共16纵行 | |
| B. | X2+的核外电子数目为18,则X在第四周期第ⅡA族 | |
| C. | Li是最活泼金属,F是最活泼非金属 | |
| D. | NaOH碱性比KOH强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸酸与氢氧化钡反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 过量CO2通入NaOH溶液中 CO2+OH-=H CO3- | |
| C. | 硝酸银溶液中加入铜粉 Ag++Cu═Cu2++Ag↓ | |
| D. | 锌与稀硝酸反应 Zn+2H+═Zn2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO、H2S的转化率之比为1:1 | |
| B. | 达平衡后H2S的体积分数为29.4% | |
| C. | 升高温度,COS浓度减小,表明该反应是吸热反应 | |
| D. | 恒温下向平衡体系中再加入CO、H2S、COS、H2各1 mol,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 3.3 | 9.7 | 6.7 | 8.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| pH | Fe3+ | Zn2+ | Mn2+ | Cu2+ |
| 开始沉淀 | 1.9 | 6.0 | 8.1 | 4.7 |
| 沉淀完全 | 3.7 | 8.0 | 10.1 | 6.7 |
| 沉淀溶解 | 不溶解 | 10.5 | 不溶解 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
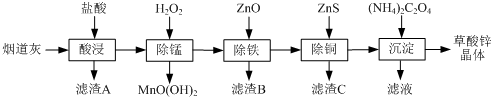
 以黄铜矿精矿为原料,制取金属铜的工艺如下所示:
以黄铜矿精矿为原料,制取金属铜的工艺如下所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
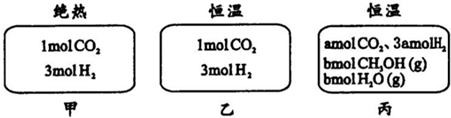
| A. | 刚开始反应时速率:甲<乙 | B. | 平衡后反应放热:甲>乙 | ||
| C. | 500℃下该反应平衡常数:K=3×102 | D. | 若a≠0,则0.9<b<l |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com