

| ||
| ||


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
| A、1mol/L的NaOH溶液中Na+的物质的量为1mol |
| B、28g乙烯所含共用电子对数目为4NA |
| C、常温常压下,32g O2与O3的混合气体中含有的原子总数为2NA |
| D、1mol苯中含有碳碳双键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
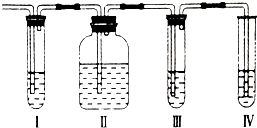 在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题:
在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题:| 光照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| SO3 | 1mol | 3mol | 3mol | 0mol |
| SO2 | 2mol | 1.5mol | 0mol | 6mol |
| O2 | 2mol | 1mol | 0mol | 5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:| △ |
| △ |
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下,可逆反应xA+yB?zC达到平衡.若:
在一定条件下,可逆反应xA+yB?zC达到平衡.若:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)用FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(1)用FeCl3溶液腐蚀印刷电路铜板的化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:
 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A、0.15mol CuO |
| B、0.1mol CuCO3 |
| C、0.075mol Cu(OH)2 |
| D、0.05mol Cu2(OH)2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com