

| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 1 mol Zn与足量的该硫酸反应产生2 g氢气 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50.0 mL | |
| D. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L |
分析 A.根据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度;
B.锌与足量浓硫酸反应开始生成的气体为二氧化硫;
C.根据溶液稀释前后溶质物质的量不变计算所需浓硫酸的体积;
D.硫酸与等质量的水混合,混合后溶液的质量为原硫酸的2倍,稀释后溶液的密度减小,故稀释后所得溶液的体积大于原硫酸体积的2倍,根据稀释定律判断.
解答 解:A.该浓H2SO4的物质的量浓度为:c=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,故A正确;
B.锌与足量浓硫酸反应开始生成的气体为二氧化硫,不生成氢气,故B错误;
C.根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,则xmL×18.4mol/L=200mL×4.6mol/L,解得:x=50,所以应量取的浓硫酸体积是50mL,故C正确;
D.硫酸与等质量的水混合,混合后溶液的质量为原硫酸的2倍,稀释后溶液的密度减小,故稀释后所得溶液的体积大于原硫酸体积的2倍,则稀释后所得溶液的浓度小于9.2mol/L,故D错误;
故选AC.
点评 本题考查溶液浓度的计算和大小比较,题目难度中等,明确物质的量浓度与溶质质量分数的关系为解答关键,注意硫酸的浓度越大,密度越大,试题有利于培养学生的分析能力及化学计算能力.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 主链上有6个碳的庚烷有3种 | |
| B. | 主链4个碳,可能只含一个支链 | |
| C. | 主链5个碳,支链可以只含乙基,也可以只含甲基 | |
| D. | 主链为3个碳时,支链形成的同分异构体含两个乙基支链,碳架结构为: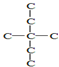 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
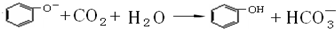 ,该反应说明苯酚具有的性质是弱酸性.
,该反应说明苯酚具有的性质是弱酸性.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NaBr+Cl2=2CaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2=2H2O+3S↓ | |
| D. | 2CO+O2=2CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡与硫酸反应:OH-+H+═H2O | |
| B. | 氧化铜与盐酸反应:O2-+2H+═H2O | |
| C. | 铁片插入硝酸银溶液中:Fe+Ag+=Fe2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 负极反应中有CO2生成 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 质子通过交换膜从负极区移向正极区 | |
| D. | 正极反应为:O2+4e-+2H2O=4OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com