
【题目】下列有关说法正确的是
A. 298 K时,2H2S(g)+SO2(g)===3S(s)+2H2O(l)能自发进行,则其ΔH>0
B. 氨水稀释后,溶液中c(NH4+)/c(NH3·H2O)的值减小
C. 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等
D. 25℃时Ka(HClO)=3.0×108,Ka(HCN)=4.9×1010,若该温度下NaClO溶液与NaCN溶液的pH相同,则c(NaClO)>c(NaCN)
【答案】D
【解析】
A.反应能自发进行,应满足H-TS<0,而该反应![]() S
S![]() 0,当H>0时不能自发进行,当
0,当H>0时不能自发进行,当![]() H
H![]() 0时低温可自发进行,该反应298K时能自发进行,故H<0,故A错误;
0时低温可自发进行,该反应298K时能自发进行,故H<0,故A错误;
B.氨水稀释后,电离平衡正向移动,![]()
![]() 的物质的量减少,
的物质的量减少,![]() 物质的量增大,因为在同一溶液中,二者的浓度比等于物质的量比,所以该比值增大,故B错误;
物质的量增大,因为在同一溶液中,二者的浓度比等于物质的量比,所以该比值增大,故B错误;
C.阳极粗铜中含有铁、锌、金、铂等金属,阳极为Zn、Fe、Cu失电子,电极反应为Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,阴极为Cu2+得电子还原成Cu,则电解过程中阳极质量减少与阴极质量增加不一定相同,故C错误;
D.25℃时, Ka(HClO)=3.0![]() ,Ka(HCNO)=4.9
,Ka(HCNO)=4.9![]() 时,HClO溶液的酸性大于HCN,根据越弱越水解原理,该温度下NaClO溶液与NaCN溶液pH相同,c(NaClO)
时,HClO溶液的酸性大于HCN,根据越弱越水解原理,该温度下NaClO溶液与NaCN溶液pH相同,c(NaClO)![]() c(NaCN),故D正确;
c(NaCN),故D正确;
本题答案为D。


科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:

(1)上述反应中生成二氧化硫的化学方程式为__。
(2)乙同学认为还可能产生氢气的理由是__。
(3)丙同学在安装好装置后,必须首先进行的一步操作是__。
(4)A中加入的试剂可能是__,作用是__;B中加入的试剂可能是__,作用是__;E中加入的试剂可能是__,作用是__。
(5)可以证明气体X中含有氢气的实验现象是:
C中:__,
D中:__。
如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?__(填“能”或“不能”),原因是_。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。
上述物质有如图转化关系:

下列说法错误的是
A. 四种元素形成的单质中W的氧化性最强
B. 甲、乙、丙中沸点最高的是丙
C. 甲常用作致冷剂
D. 甲、乙分子均只含极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式书写不正确的是
A. 用铜电极电解MgCl2溶液:Mg2++2Cl-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑
Mg(OH)2↓+Cl2↑+H2↑
B. 饱和碳酸钠溶液中通入足量的二氧化碳:2Na++CO32-+CO2+H2O=2NaHCO3↓
C. 向Ba(OH)2溶液中加入NaHSO4至溶液为中性:Ba2++2OH-+2H++![]()
![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84g/cm3)配制l00mL 1mol/L的稀硫酸,现绐出下列仪器(配制过程中可能用到):①100mL量筒②10mL量筒③50mL烧杯 ④托盘天平⑤100mL容量瓶⑥胶头滴管⑦玻璃棒,配制中使用仪器的先后順序排列正确的是
A. ④③⑦⑤⑥ B. ②⑤⑦⑥ C. ①③⑤⑥⑦ D. ②⑥③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活、环境保护、资源利用等密切相关,下列说法正确的是
A. 大米、玉米、小麦中的淀粉经水解可变成乙醇
B. 利用二氧化碳制造全降解塑料,可以缓解温室效应
C. 测定氢氧化钠的熔点时,可以将氢氧化钠固体放入石英坩埚中高温加热
D. 海洋中含有丰富的矿产资源,仅利用物理方法可以获得![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。下列说法正确的是( )

A. 反应物微粒是S、SO![]() 、OH-
、OH-
B. 该反应可能在酸性条件下进行
C. 氧化剂与还原剂的物质的量之比为2∶1
D. 2 mol S参加反应时,转移的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,常用O2氧化HCl转化成Cl2,提高效益,减少污染。反应为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
c(Cl2)/10-3molL-1 | 0 | 1.8 | 3.7 | 5.4 | 7.2 | 7.2 |
下列说法错误的是( )
A.条件不变时,12min时v正(Cl2)=v逆(H2O)
B.2.0~4.0min内的平均反应速率大于6.0~8.0min内的
C.0~8.0min内HCl的平均反应速率为1.8mol·L-1·min-1
D.加入高效催化剂,达到平衡所用时间小于8.0min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和砷均为重要的无机材料,在化工领域具有广泛的应用。
(1)基态As原子的价层电子的电子云轮廓图形状为________。同一周期As、Ge、Se三种元素的第一电离能由大到小的顺序为________________。
(2)Na3AsO3中所含阴离子的立体构型为___________,写出一个与AsO33-具有相同空间构型和键合形式的分子____________________(填化学式)。
(3)在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子和N原子轨道的杂化类型分别为__________,_________;1mol尿素分子中,![]() 键的数目为___________。
键的数目为___________。
(4)N2H4是火箭的燃料,与氧气的相对分子质量相同,它在常温常压下是液态,而氧气是气态,造成这种差异的主要原因是__________________。
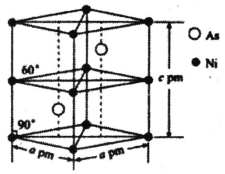
(5)某砷镍合金的晶胞结构如图所示,阿伏加德罗常数的值为NA,则该晶体的密度![]() =________g·cm-3,该晶体中与每个Ni原子距离最近的As原子有_______个。
=________g·cm-3,该晶体中与每个Ni原子距离最近的As原子有_______个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com