
【题目】M,N,X,Y四种短周期主族元素在元素周期表中的相对位置如图所示.已知它们的原子序数总和为48,则下列有关说法中不正确的是( ) ![]()
A.N与X位于元素周期表中ⅥA族
B.M,X,Y三种元素的最高价氧化物对应的水化物均为强酸
C.M,N,X,Y均位于金属与非金属的分界线上
D.M的气态氢化物与Y的气态氢化物反应,可生成离子化合物
【答案】C
【解析】解:由M、N、X、Y四种短周期主族元素在元素周期表中的相对位置,可知M、N处于第二周期,X、Y处于第三周期,令N的原子序数为a,则M原子序数为a﹣1,X原子序数为a+8,Y原子序数为a+9,四元素原子序数总和为48,则a﹣1+a+a+8+a+9=48,解得a=8,故N为O元素、M为N元素、X为S元素、Y为Cl,A.N为O元素、X为S元素,二者位于元素周期表中ⅥA族,故A正确;
B.M、X、Y三种元素的最高价氧化物对应的水化物分别为硝酸、硫酸、高氯酸,均为强酸,故B正确;
C.O、N、S、Cl均不位于金属与非金属的分界线上,故C错误;
D.氨气与氯化氢反应得到氯化铵,氯化铵由铵根离子与氯离子构成,属于离子化合物,故D正确,
故选C.


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】高锰酸钾在不同的条件下发生的反应如下:MnO ![]() +5e﹣+8H+═Mn2++4H2O ①
+5e﹣+8H+═Mn2++4H2O ①
MnO ![]() +3e﹣+2H2O═MnO2↓+4OH﹣②
+3e﹣+2H2O═MnO2↓+4OH﹣②
MnO ![]() +e﹣═MnO42﹣(溶液绿色)③
+e﹣═MnO42﹣(溶液绿色)③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的影响.
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为→ .
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2,完成下列化学方程式(横线上填系数,括号内填物质):①KMnO4+K2S+═K2MnO4+K2SO4+S↓+ .
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水晒盐的原理是( )
A.海水分解
B.温度升高,其他溶质的溶解度增大
C.升高温度,降低食盐在水中的溶解度
D.利用阳光、风力蒸发水分使氯化钠成晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,可行的是
A. 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铁粉
B. 用萃取的方法分离汽油和煤油
C. 用溶解和过滤的方法分离硝酸钾和氯化钠固体混合物
D. 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若aXm+与bYn-的核外电子排布相同,下列关系式正确的是( )
A. b=a-n+mB. b=a-n-m
C. 离子半径Xm+<Yn+D. 原子半径X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是
A.用溴水可鉴别苯、CCl4、苯乙烯
B.加浓溴水,然后过滤可除去苯中少量己烯
C.苯、溴水、铁粉混合制成溴苯
D.可用分液漏斗分离溴乙烷和甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图. 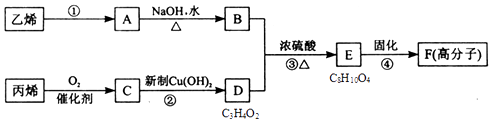
关于该过程的相关叙述正确的是( )
A.反应④的反应类型是加聚
B.物质A含有两种官能团
C.物质B催化氧化后可以得到乙醛
D.1mol物质D最多可以消耗2molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节.回答下列问题: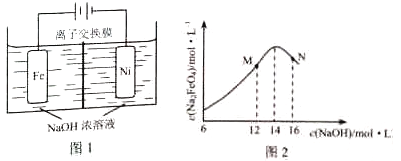
(1)与汽油相比,氢气作为燃料的优点是(至少答出两点).但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式: .
(2)氢气可用于制备H2O2 . 已知:
H2(g)+A(l)═B(l)△H1
O2(g)+B(l)═A(l)+H2O2(l)△H2
其中A、B为有机物,两反应均为自发反应,则H2(g)+O2(g)═H2O2(l)的△H=0(填“>”或“=”)
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)MHx+2y(s)△H<0达到化学平衡.下列有关叙述正确的是
a.容器内气体压强保持不变
b.吸收ymol H2只需1molMHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为 .
(5)化工生产的副产氢也是氢气的来源,电解法制取有广泛用途的Na2FeO4 . 同时获得氢气:Fe+2H2O+2OH﹣→FeO42﹣+3H2↑,装置如图所示,装置通电后,铁电极附近生成紫红色FeO42﹣ , 镍电极有气泡产生.若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质.
已知:Na2FeO4只在强碱性条件下稳定,易被H2还原.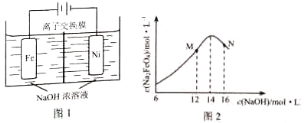
①电解一段时间后,c(OH﹣)降低的区域在(填“阴极室”或“阳极室”).
②电解过程中,须将阴极产生的气体及时排出,其原因为 .
③c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀,滤液与4molL﹣1NaOH溶液时恰好完全中和.试求:
(1)混合液H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液稀释至80mL,加入1.92g铜粉共热时,收集到气体在标准状况下的体积为多少毫升?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com