
| A. | 加入催化剂一定能加快反应速率 | B. | 温度越高反应速率也越大 | ||
| C. | 固体颗粒大小也会影响反应速率 | D. | 反应速率主要由反应物性质决定 |
分析 使用正催化剂、升高温度、增大压强、增大接触面积均可加快反应速率,反应物本身的性质为影响反应速率的内因,以此来解答.
解答 解:A.加入催化剂可能加快反应速率,若使用负催化剂,反应速率减小,故A错误;
B.温度升高,活化分子百分数增大,反应速率加快,故B正确;
C.增大接触面积,反应速率加快,则固体颗粒大小也会影响反应速率,故C正确;
D.反应速率主要由反应物性质决定,为内因,而温度、浓度、压强均为影响反应速率的外因,故D正确;
故选A.
点评 本题考查化学反应速率的影响因素,为高频考点,把握常见的影响速率的外因为解答的关键,侧重分析与应用能力的考查,注意影响速率的内因与外因不同,注重迁移应用能力的训练,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氟离子的结构示意图: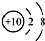 | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | 溴化铵的电子式: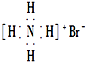 | |
| D. | 质子数为53,中子数为78的碘原子:53131 I |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5%H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
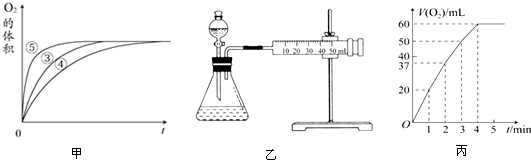
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
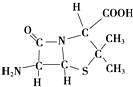 人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、聚乙烯、二氧化硅等17种“分子”改变过人类的世界.
人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、聚乙烯、二氧化硅等17种“分子”改变过人类的世界.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加铁粒质量 | B. | 换成同浓度的稀硫酸 | ||
| C. | 改成98%的浓硫酸 | D. | 加入纯硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
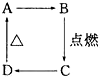 如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.
如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某种核素的相对原子质量 | |
| B. | 某种核素的原子质量 | |
| C. | 某种元素的平均相对原子质量 | |
| D. | 某种元素的平均相对原子质量的近似值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com