
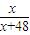 =40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与1.204×1023个H2完全反应,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素.结合物质性质与元素周期律解答.
=40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与1.204×1023个H2完全反应,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素.结合物质性质与元素周期律解答. =40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与1.204×1023个H2完全反应,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素.
=40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与1.204×1023个H2完全反应,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素. Na2O2.过氧化钠与二氧化碳反应生成碳酸钠与氧气,反应方程式为2Na2O2+2CO2═2Na2CO3+O2.
Na2O2.过氧化钠与二氧化碳反应生成碳酸钠与氧气,反应方程式为2Na2O2+2CO2═2Na2CO3+O2. Na2O2;2Na2O2+2CO2═2Na2CO3+O2.
Na2O2;2Na2O2+2CO2═2Na2CO3+O2.

科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
有短周期A、B、C、D、E五种元素,它们的原子序数由A至E渐大。D的氢化物的分子式为H2D,D的最高价氧化物中D的质量分数为40%,且D原子的原子核中质子数和中子数相等。A原子最外电子层上有4个电子。B的阴离子与C的阳离子和氖原子的电子层结构相同。E原子的M电子层上共有7个电子。常温常压下,B单质是气体,已知0.1mol的B单质与1.204×1023个H2完全反应。C单质在加热条件下与B单质反应生成淡黄色固体。根据上述情况,试回答下列各问题。
(1)A~E的元素符号分别为______、______、______、______、______。
(2)C单质和B单质在加热条件下生成化合物A2B2,写出反应的化学方程式:
_______________________________________;
写出A2B2与A的氧化物反应的化学方程式:
_______________________________________。
(3)试写出D、E最高价氧化物水化物分子式_________,_________,并比较酸性强弱________________;写出D、E气态氢化物分子式___________、___________,比较它们的稳定性________________。
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源: 题型:
有短周期A、B、C、D、E五种元素,它们的原子序数由A至E渐大。D的氢化物的分子式为H2D,D的最高价氧化物中D的质量分数为40%,且D原子的原子核中质子数和中子数相等。A原子最外电子层上有4个电子。B的阴离子与C的阳离子和氖原子的电子层结构相同。E原子的M电子层上共有7个电子。常温常压下,B单质是气体,已知0.1mol的B单质与1.204×1023个H2完全反应。C单质在加热条件下与B单质反应生成淡黄色固体。根据上述情况,试回答下列各问题。
(1)A~E的元素符号分别为______、______、______、______、______。
(2)C单质和B单质在加热条件下生成化合物A2B2,写出反应的化学方程式: _________________________;
写出A2B2与A的氧化物反应的化学方程式: _______________________________________。
(3)试写出D、E最高价氧化物水化物分子式_________,_________,并比较酸性强弱________________;写出D、E气态氢化物分子式___________、___________,比较它们的稳定性________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com