
【题目】(1)常温下,向20mL0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。回答下列问题
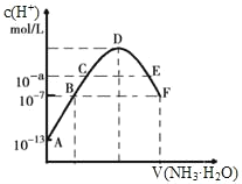
①NaHB溶液呈_______(填“酸性”“碱性”或“中性”)
②A、D、E三点溶液的pH由大到小为:_______
③F点溶液c(NH4+)_______2c(B2-)(填“>”“<”或“=”)
(2)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量Mg(OH)2沉淀。
①分别向两支试管中加入不同试剂,请填写下表中的实验现象(用下列选项中字母代号填写)
试管编号 | 加入试剂 | 实验现象 |
Ⅰ | 2滴0.1mol/LFeCl3溶液 | _______ |
Ⅱ | 4mL2mol/LNH4Cl溶液 | _______ |
A 白色沉淀转化为红褐色沉淀 B 白色沉淀不发生改变
C 红褐色沉淀转化为白色沉淀 D 白色沉淀溶解,得无色溶液
②同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的沉淀溶解平衡正向移动。猜想2:_______。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明正确的是_______(填“猜想1”或“猜想2”)。
【答案】酸性 E>D>A = A D NH4Cl水解出来的H+与Mg(OH)2电离出OH-结合成水,使Mg(OH)2的沉淀溶解平衡正向移动 猜想1
【解析】
(1) ①未加入氨水前,溶液的水电离出的OH-浓度为10-13mol/L,所以溶液中c(H+)=0.1mol/L,该酸的浓度为0.05mol/L,所以该酸为二元强酸;
②酸、碱对水的电离起抑制作用,可水解的盐对水的电离起促进作用,随着氨水的不断滴入,溶液中水电离的c(H+)逐渐增大,当两者恰好完全反应生成(NH4)2B时水的电离程度达最大(图中D点),继续加入氨水,水电离的c(H+)逐渐减小;
③溶液中的电荷守恒,可得到答案;
(2)(3)根据已知数据,求出两种物质的物质的量,可确定反应是否完全,再结合Ksp的大小,可判断出沉淀转化的本质,是由Ksp的大小引起的,还是发生其它反应生成的;沉淀的溶解要根据物质的性质来确定,Mg(OH)2属于弱碱,能够与NH4+水解生成的H+发生中和反应而溶解,也能够与NH4+发生复分解反应,生成弱电解质NH3·H2O而溶解,要验证溶解的原因,可用含NH4+的中性溶液做对比实验。
(1) ①NaHB属于强酸的酸式盐,NaHB溶液应该呈酸性,故答案为:酸性;
②向酸溶液中逐渐加入碱发生中和反应,混合液溶液的pH是逐渐增大的,而A显酸性,最小,pH由大到小为E>D>A,故答案为E>D>A;
③D.F点溶液由(NH4)2B和氨水混合而成,由于水电离的c(H+)=1×10-7mol/L,溶液中H+全部来自水电离,则F点水溶液呈中性,此时溶液中的电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(B2-),因c(H+)=c(OH-),所以有c(NH4+)=2c(B2-),故答案为:=;
(2) ①已知n(MgCl2)=1×10-3L×0.1mol/L=1×10-4mol,n(NaOH)≈0.1×10-3L×2mol/L=2×10-4mol,由反应Mg2++2OH-=Mg(OH)2↓可知,二者基本反应完全,生成白色沉淀Mg(OH)2,当向其中加入FeCl3溶液时,由于Ksp[Fe(OH)3]=4.0×10-38远小于Ksp[Mg(OH)2]=1.8×10-11,所以白色沉淀Mg(OH)2转化为红褐色沉淀Fe(OH)3,故答案选A;当向其中加入NH4Cl溶液,NH4+与Mg(OH)2电离出的OH-结合生成弱电解质NH3·H2O,使Mg(OH)2的溶解平衡正向移动,最终使Mg(OH)2完全溶解得无色溶液,所以答案选D;
②NH4Cl因水解而呈酸性,生成的H+与Mg(OH)2电离出OH-结合生成水,使Mg(OH)2的溶解平衡正向移动,故答案为:NH4Cl水解出来的H+与Mg(OH)2电离出OH-结合成水,使Mg(OH)2的沉淀溶解平衡正向移动;
(3)由于醋酸铵溶液(pH=7)呈中性,能使Mg(OH)2沉淀溶解,说明不是NH4+水解呈酸性导致Mg(OH)2溶解;当加入弱碱性的NH4Cl和氨水混合液(pH=8)时,沉淀也溶解,说明猜想2是错误的。因此证明Mg(OH)2沉淀溶解的根本原因是NH4+与Mg(OH)2电离出OH-结合生成弱电解质NH3·H2O,促进Mg(OH)2溶解平衡正向移动,最终得无色溶液,所以猜想1是正确的,故答案为:猜想1。


科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
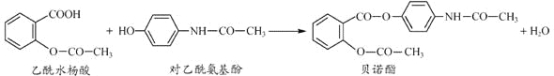
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
(1)K3[Fe(CN)6]中Fe3+与CN-之间的作用为___,该化学键能够形成的原因是___。
(2)某有机物的结构简式为![]() 。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为___。
。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为___。
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___。
(4)NH4Cl中阳离子中心原子的价层电子对数为___,该物质中不含有___。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键 E.σ键 F.π键
(5)NCl3的立体构型为___,其中心原子的杂化轨道类型为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( )
a.体积②>③>①>④
b.密度②>③>④>①
c.质量②>③>①>④
d.氢原子个数①>③>④>②
A.abcB.bcdC.abdD.abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由MnS矿(还含少量FeCO3、MgO等)制备高纯硫酸锰,工艺如图所示:
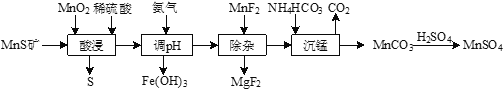
已知相关金属离子(浓度为0.1mol·L-1)形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Mg2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.8 | 8.9 |
沉淀完全的pH | 10.1 | 8.3 | 3.2 | 10.9 |
(1)“酸浸”过程中,MnS(难溶)发生反应的离子方程式为_____________。
(2)“酸浸”时MnO2应过量,目的是____________和将Fe2+氧化为Fe3+。
(3)已知Ksp[Fe(OH)3]=4×10-38。常温下,当溶液的pH=2时,c(Fe3+)=______________mol·L-1。
(4)“除杂”时若溶液pH过低,Mg2+沉淀不完全,原因是_______________。
(5)“沉锰”反应的化学方程式为_____________。

(6)用MnO2悬浊液吸收SO2也可以制取MnSO4。将SO2和空气的混合气通入MnO2悬浊液,测得吸收液中Mn2+、SO42-的浓度随反应时间t变化如图。导致Mn2+、SO42-浓度变化产生明显差异的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种药物合成中间体,其合成路线如下:
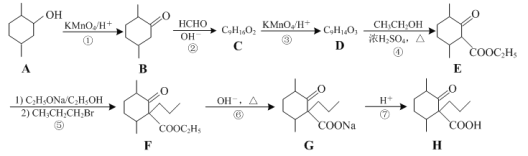
(1)A→B的反应的类型是____________反应。
(2)化合物H中所含官能团的名称是____________和____________。
(3)化合物C的结构简式为___________。B→C反应时会生成一种与C互为同分异构体的副产物,该副产物的结构简式为___________。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:____________。
①能发生水解反应,所得两种水解产物均含有3种化学环境不同的氢;
②分子中含有六元环,能使溴的四氯化碳溶液褪色。
(5)已知:![]() CH3CH2OH。写出以环氧乙烷(
CH3CH2OH。写出以环氧乙烷(![]() )、
)、![]() 、乙醇和乙醇钠为原料制备
、乙醇和乙醇钠为原料制备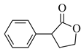 的合成路线流程图_______________(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图_______________(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对FeCl3分别与Na2SO3、NaHSO3的反应进行探究。
(甲同学的实验)
装置 | 编号 | 试剂X | 实验现象 |
| I | Na2SO3溶液(pH≈9) | 闭合开关后灵敏电流计指针发生偏转 |
II | NaHSO3溶液(pH≈5) | 闭合开关后灵敏电流计指针未发生偏转 |
(1)怎样配制FeCl3溶液? ________________________________________________________。
(2)甲同学探究实验I的电极产物。
① 取少量Na2SO3溶液电极附近的混合液,加入_________________________________,产生白色沉淀,证明产生了SO42-。
② 该同学又设计实验探究另一电极的产物,其实验方案为_______________________________。
(3)实验I中负极的电极反应式为______________________________________________________。
乙同学进一步探究FeCl3溶液与NaHSO3溶液能否发生反应,设计、完成实验并记录如下:
装置 | 编号 | 反应时间 | 实验现象 |
| III | 0~1 min | 产生红色沉淀,有刺激性气味气体逸出 |
1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | ||
30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
(4)乙同学认为刺激性气味气体的产生原因有两种可能,用离子方程式表示②的可能原因。
① Fe3++3HSO3-![]() Fe(OH)3 +3SO2;②_____________________________________________。
Fe(OH)3 +3SO2;②_____________________________________________。
![]()
从反应速率和化学平衡两个角度解释1~30 min的实验现象:______________________________。
(实验反思)
(6)分别对比I和II、II和III,FeCl3能否与Na2SO3或NaHSO3发生氧化还原反应和______________________有关(写出两条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com