
| A、此法的优点之一是原料来源丰富 |
| B、进行①②③步骤的目的是从海水中提取氯化镁 |
| C、第④步电解制镁是由于镁是很活泼的金属 |
| D、以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应 |
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验中所用到的锥形瓶和容量瓶,在洗涤后均需要润洗 |
| B、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,最终氢氧化钠溶液浓度将偏大 |
| C、滴定时,左手提酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视滴定管内液面变化 |
| D、中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6 g |
| B、2.4 g |
| C、3.2 g |
| D、4.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
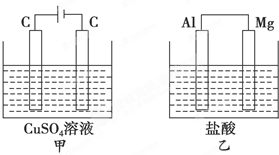 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )| A、溶液的质量变化:甲减小乙增大 |
| B、溶液pH变化:甲减小乙增大 |
| C、相同条件下产生气体的体积:V甲=V乙 |
| D、电极反应式:甲中阴极为Cu2++2e-═Cu,乙中负极为Mg-2e-═Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 以铬酸钾((K2CrO4))为原料,用电化学法制备铬酸钾(K2CrO4)的实验装置如图,其反应原理可表示为4Kr2CrO4+4H2O
以铬酸钾((K2CrO4))为原料,用电化学法制备铬酸钾(K2CrO4)的实验装置如图,其反应原理可表示为4Kr2CrO4+4H2O| 通电 |
| A、在阴极室,随着反应的进行溶液的pH逐渐变小 |
| B、不锈钢电极上生成O2,惰性电极上得到H2 |
| C、惰性电极发生的电极反应为2H2O-4e-═4H++O2↑ |
| D、不锈钢应连接直流电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进入煤矿井下作业,戴上安全帽,用帽上的矿灯照明 |
| B、节日期间,可以在热闹繁华的商场里燃放烟花爆竹,欢庆节日 |
| C、点燃打火机,可以检验液化气钢瓶口是否漏气 |
| D、实验室里,可以将水倒入浓硫酸及时用玻璃棒搅拌,配制稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| △ |
| A、4种 | B、5种 | C、6种 | D、7种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com