
| A. | 8.5g | B. | 10.8g | C. | 6.2g | D. | 4.6g |
分析 设出钠块中钠、氧化钠的物质的量,分别根据总质量、钠元素守恒列式计算出氧化钠的物质的量,最后m=nM计算出氧化钠的质量.
解答 解:1L 0.4mol•L-1的NaOH溶液中含有NaOH的物质的量为:0.4mol/L×1L=0.4mol,
设该钠块中含有钠、氧化钠的物质的量分别为x、y,
则:23x+62y=10.8、x+2y=0.4,
联立解得:x=0.2、y=0.1mol,
则原固体中氧化钠的质量为:62g/mol×0.1mol=6.2g,
故选C.
点评 本题考查了混合物反应的计算,题目难度中等,明确物质的量与摩尔质量、物质的量浓度的关系为解答关键,注意掌握质量守恒定律在化学计算中的应用方法.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用铝槽密闭盛装浓硫酸 | |
| B. | 工业上利用蛋白质的水解反应生产肥皂和甘油 | |
| C. | 乙醇可用作汽车燃料 | |
| D. | 食醋可用于消除暖水瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
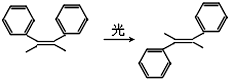
| A. | 分子式相同,互为同分异构体 | |
| B. | 均可发生加聚反应、氧化反应 | |
| C. | 均含有苯环,都是苯的同系物 | |
| D. | 分子中所有碳原子均可能处于同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量g•mol-1 | B. | 物质的量浓度L•mol-1 | ||
| C. | 气体摩尔体积L•mol-1 | D. | 物质的量mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 橱名 | 甲 | 乙 | 丙 | 丁 |
| 试剂 | 盐酸、硝酸 | 烧 碱、苛性钾 | 食盐、氯化钡 | 酒精、汽油 |
| A. | 甲橱 | B. | 乙橱 | C. | 丙橱 | D. | 丁橱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能使化学反应速率加快,平衡常数增大 | |
| B. | 平衡常数随温度的改变而改变 | |
| C. | 化学平衡发生移动,平衡常数必发生变化 | |
| D. | 对于3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为K=$\frac{c(F{e}_{3}{O}_{4})•{c}^{4}({H}_{2})}{c(Fe)•{c}^{4}({H}_{2}O)}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com